Wirkstoffdesign und Optimierung
Prof. Dr. Anna K. H. Hirsch
Die Hirsch-Gruppe verfolgt eine strukturbasierte rationale Designstrategie, bei der sie sich auf biologisch relevante, häufig wenig erforschte Enzyme, Transporter und Regulatoren aus Bakterien oder Parasiten konzentriert. Die Gruppe verwendet diverse biophysikalische Methoden, um Wechselwirkungen zwischen Substanzen und ihren Zielproteinen zu untersuchen, und setzt zahlreiche in vitro- und zellbasierte Assays zur Evaluierung neuartiger Anti-Infektiva ein. Basierend auf diesen Ergebnissen erfolgt die Multiparameter-Optimierung der Wirkstoffe.
Unsere Forschung
Die Krise der antimikrobiellen Resistenz erfordert dringend die Entwicklung neuer antibakterieller Wirkstoffe mit neuartigen Wirkmechanismen. Um dies zu erreichen, verfolgen wir eine zielgerichtete Strategie, die sich auf ein vielfältiges Portfolio biologisch relevanter, wenig erforschter Wirkstoffziele konzentriert, darunter Enzyme, Transporter und Regulatoren in bakteriellen Krankheitserregern. Diese Zielmoleküle lassen sich in zwei Hauptkategorien einteilen: solche, die lebenswichtige Mechanismen innerhalb der Bakterien beeinträchtigen und zu deren Tod führen (z. B. DXPS, ECF-T, DnaN), und Pathoblocker, die die Pathogenität und Virulenz beeinträchtigen, ohne die Lebensfähigkeit der Bakterien zu beeinträchtigen (z. B. ColH, LasB). Man geht davon aus, dass die Pathoblocker eine geringere Resistenzentwicklung bewirken, während die kommensale Mikrobiota erhalten bleibt.
Wir setzen eine Reihe von Strategien zur Identifizierung von Hits ein, darunter struktur- und fragmentbasiertes Wirkstoffdesign, virtuelles Screening, Hochdurchsatzscreening und eine Vielzahl biophysikalischer Methoden. Darüber hinaus leisten wir Pionierarbeit bei innovativen, auf Proteinen basierenden Techniken wie der dynamischen kombinatorischen Chemie und der kinetischen, zielgerichteten Synthese, um wichtige Engpässe bei der Arzneimittelentdeckung zu beseitigen. Wir verwenden klassische und innovative medizinisch-chemische Ansätze, um die vielversprechendsten Inhibitoren zu entwerfen, zu synthetisieren und zu profilieren, was eine effiziente anschließende Optimierung mit mehreren Parametern ermöglicht. Verschiedene in vitro und zellbasierte Assays, die Generierung von in silico Daten, die Aufklärung der Wirkungsweise und die Co-Kristallisation ausgewählter Verbindungen mit ihren Zielmolekülen unterstützen die unkomplizierte Bewertung neuartiger Antiinfektiva und deren weitere Optimierung.
Unser interdisziplinäres Team besteht aus Wissenschaftlern mit unterschiedlichem Hintergrund, wie z.B. synthetische organische oder medizinische Chemie, Pharmazie, Pharmakologie, Biologie oder Biochemie, was es uns ermöglicht, unsere interdisziplinären Projekte zu bearbeiten.
Team-Mitglieder

Prof. Dr. Anna K. H. Hirsch
Gruppenleiterin

Bahareh Kadkhodazadeh
Assistentin

Nicole Klein Ramos
Assistentin

Dr. Andreas Kany
Wissenschaftler

Dr. Jörg Haupenthal
Wissenschaftler

Dr. Mostafa Hamed
Wissenschaftler

Dr. Ayanda Zulu
Postdoc

Dr. Charlotte O’Donnell
Postdoc

Dr. Diletta Bergamo
Postdoc

Angeliki Vgenopoulou
Doktorandin

Faraz Qurban
Doktorand

Gabriele Bianchi
Doktorand

Lukas Hiller
Doktorand

Niklas Krappel
Doktorand

Niklas Wirschem
Doktorand

Paul Blanchart
Doktorand

Walid Shahrour
Doktorand

Jannine Seelbach
Technische Assistentin

Jeannine Jung
Technische Assistentin

Simone Amann
Technische Assistentin

Tabea Wittmann
Technische Assistentin
Forschungsprojekte
Nachstehend folgt ein Überblick über ausgewählte Zielmoleküle, an denen wir derzeit unter Anwendung der oben beschriebenen Strategien arbeiten:
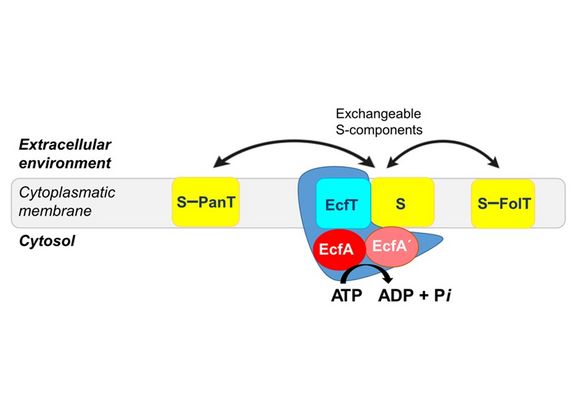
ECF-T
Die Energy-Coupling-Factor-Transporter (ECF-T) sind eine Familie von Transmembranproteinen, die an der Aufnahme von Vitaminen durch ein breites Spektrum von Bakterien beteiligt sind. Die Hemmung der Aktivität dieser Proteine verringert die Lebensfähigkeit von Organismen, die auf die Vitaminaufnahme angewiesen sind, einschließlich pathogener Arten wie Streptococcus pneumoniae, Enterococcus faecium und Staphylococcus aureus. Da mehrere Bakterien wichtige Vitamine wie Folsäure, Pantothenat und Niacin nicht de novo synthetisieren können, sind sie auf ECF-T angewiesen, um sie aus der Umwelt aufzunehmen. Aufgrund dieser zentralen Rolle im Stoffwechsel von Bakterien sind ECF-T neuartige, vielversprechende antimikrobielle Zielstrukturen zur Bekämpfung von Infektionen. Vor kurzem haben wir mehrere Klassen von ECF-T-Inhibitoren als potenzielle antibakterielle Wirkstoffe identifiziert. Wir entwickeln diese Verbindungen derzeit mit Unterstützung eines ERC Proof-of-Concept Grants weiter.
©HIPS/DDOP
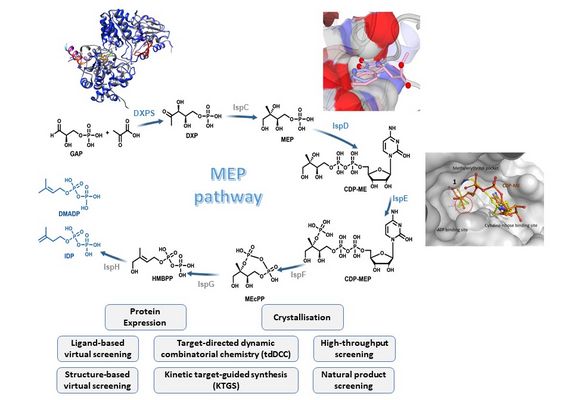
MEP PATHWAY (TARGETS: DXS, ISPD, ISPE):
Der Methyl-Erythrit-Phosphat-Stoffwechselweg (MEP) ist eine reichhaltige, noch nicht ausreichend erforschte Quelle für Antiinfektiva, die beim Menschen nicht vorkommen, aber in vielen pathogenen Bakterien, Protozoen und Pflanzen essenziell sind. Dies eröffnet die Möglichkeit, hochselektive Inhibitoren zu entwickeln, die gegen klinisch relevante Krankheitserreger wie die vier ESKAPE-Erreger wirken, die im Mittelpunkt des ersten Doktoranden-Netzwerks MepAnti stehen:Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa und Enterobacter spp., die alle nach der Globalen Prioritätenliste der WHO für antibiotikaresistente Bakterien hohe oder kritische Priorität haben - sowie Mycobacterium tuberculosis und Plasmodium falciparum. Bei diesen Erregern ist der MEP-Weg die einzige Quelle für Isopentenyldiphosphat (IDP) und Dimethylallyldiphosphat (DMADP). Letztere sind die universellen Bausteine für die Biosynthese von Isoprenoiden, einer großen und vielfältigen Klasse von Naturstoffen, die eine Vielzahl von unverzichtbaren Funktionen erfüllen. Mit DXPS, IspD und IspE haben wir drei wesentliche Enzyme dieses Weges mit ausgezeichneten Aktivitäten gegen die genannten Krankheitserreger im Visier.
DnaN
Antibakterielle Medikamente, die auf essentielle Multienzymkomplexe abzielen, sind weniger anfällig für Resistenzentwicklung, da ihre Fehlfunktion schwer zu umgehen ist. In diesem Zusammenhang enthält die bakterielle Replisom-Maschinerie, die aus mindestens zwölf interagierenden Enzymen besteht, die in Bakterien hoch konserviert sind, mehrere attraktive und vielversprechende antibakterielle Ziele - darunter die bakterielle β-Gleitklemme DnaN. DnaN ist eine wichtige Untereinheit des Holoenzyms der DNA-Polymerase III, die die Dissoziation der Polymerase verhindert und die Aktivität der Polymerase erhöht. Darüber hinaus zeigt die β-Gleitklemme Interaktionen mit einer Vielzahl anderer Enzyme, die an Replikations- und DNA-Reparaturprozessen beteiligt sind. Seine wichtige Rolle im Replikationsprozess, seine hochkonservierte Struktur bei verschiedenen Bakterienarten und seine erhebliche strukturelle Divergenz zum Gegenstück bei Säugetieren (PCNA) machen DnaN zu einem attraktiven Ziel für die Behandlung verschiedener Krankheitserreger, einschließlich M. tuberculosis. Ausgehend von dem Naturprodukt Griselimycin (GM), einem bekannten DnaN-Binder, haben wir einen halbsynthetischen Ansatz gewählt, der zu einer Reihe von GM-Derivaten mit vielversprechenden antibakteriellen Aktivitäten führte. Darüber hinaus haben wir verschiedene synthetische kleine Moleküle identifiziert, die an DnaN binden. Die Hit-to-Lead-Optimierung der vielversprechendsten Verbindungen wird derzeit von CARB-X finanziert.
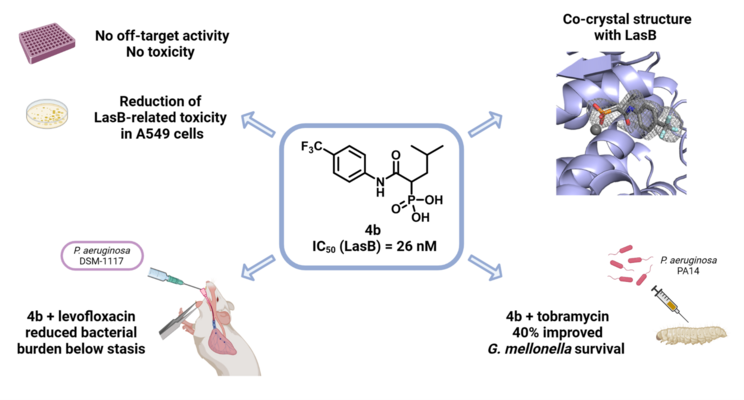
LasB
P. aeruginosa (PA), ein hochproblematischer gramnegativer Erreger, dem die WHO hohe Priorität eingeräumt hat, ist für viele nosokomiale Infektionen wie die im Krankenhaus erworbene und beatmungsassoziierte Lungenentzündung verantwortlich. Der opportunistische Erreger wird auch häufig in Verbrennungswunden, in der Lunge von COPD- und Mukoviszidose-Patienten gefunden und kann bakterielle Keratitis verursachen. Von PA abgeleitete Virulenzfaktoren spielen eine zentrale Rolle bei den Mechanismen, die seine Pathogenese und Infektiosität vermitteln. Die Strategie zur Entwicklung von „Pathoblockern“, die auf solche Virulenzfaktoren abzielen, dürfte im Vergleich zu herkömmlichen Antibiotika weniger anfällig für die Entwicklung von Resistenzen sein und das kommensale Mikrobiom schonen. Einer der wichtigsten Virulenzfaktoren von PA ist die extrazelluläre Zink-Metalloprotease Elastase LasB. LasB trägt wesentlich zum Fortschreiten der Krankheit bei PA-Infizierten bei, indem es die Invasion des Wirts und die Umgehung des Immunsystems erleichtert. Die Hemmung von LasB ist eine vielversprechende Strategie, um die Virulenz von PA wirksam zu reduzieren, ohne die Lebensfähigkeit des Erregers und das Mikrobiom des Wirts zu beeinträchtigen. Unsere vielversprechendsten LasB-Inhibitoren, die aus einer von CARB-X finanzierten Hit-to-Lead-Optimierungskampagne hervorgegangen sind, weisen nanomolare IC50-Werte, in vivo Wirksamkeit in Mausmodellen von PA-Lungeninfektionen und Keratitis sowie ein vielversprechendes Sicherheitsprofil auf und befinden sich derzeit im INCATE-Portfolio.
©HIPS/DDOP
RSV
Das Respiratory Syncytial Virus (RSV) verursacht schwere Virusinfektionen, insbesondere bei Kleinkindern, immunsupprimierten Personen und älteren Menschen. Um neue Behandlungsmöglichkeiten für RSV zu entwickeln, arbeiten wir an neuen synthetischen Wirkstoffen, die auf das Fusionsprotein (F-Protein) abzielen. Dieses Protein spielt eine zentrale Rolle beim Eintritt des Virus in die Wirtszelle und ist bei allen RSV-Untergruppen hoch konserviert. Obwohl es als Angriffspunkt für Medikamente validiert wurde, sind bisher keine niedermolekularen Inhibitoren des F-Proteins als Medikamente zugelassen. Im Rahmen eines von der Volkswagen-Stiftung geförderten interdisziplinären Projekts optimieren wir vielversprechende Gerüste für niedermolekulare Inhibitoren, die auf das RSV F-Protein abzielen, wobei der Schwerpunkt auf der strukturbasierten Multiparameter-Optimierung mittels Medizinalchemie liegt.
Publikationen
2026
An investigation of phosphinamides as a functional group for medicinal chemistry
Meurillon V, Blanchart P, Ullah V, Chan D, Perry M (2026)
Med Chem Res 35 (1): 118-134DOI: 10.1007/s00044-025-03498-y
Exploring the Role of Pseudomonas aeruginosa Elastase in Lung Epithelial Barrier Dysfunction: Advancing toward Antivirulence Therapies
Shafiei R, Alhayek A, Hiller L, Latta L, Neu T, Aljohmani A, Abdollahibiroun S, Schönborn E, Yildiz D, Schneider-Daum N, …, Haupenthal J, Hirsch A (2026)
ACS Infect. Dis.DOI: 10.1021/acsinfecdis.5c00915
Identification of a new protein-RNA interaction inhibitor targeting the KH34 region of the insulin-like growth factor 2 mRNA binding protein 2 (IGF2BP2/IMP2)
Berwanger A, Wagner K, Both S, Kany A, Mazlom K, Hirsch A, Kiemer A, Empting M (2026)
European journal of medicinal chemistry 307DOI: 10.1016/j.ejmech.2026.118624
Multiparameter Optimization of Pseudomonas aeruginosa Elastase Inhibitors for Systemic Administration
Abdelsamie A, Konstantinovic J, Kany A, Schütz C, Kolling D, Speicher S, Klein A, Shafiei R, Bouté M, Mundry K, …, Haupenthal J, Hirsch A (2026)
Journal of medicinal chemistry 69 (4): 4160-4186DOI: 10.1021/acs.jmedchem.5c02788
Design of Poly-Catechol Biodynamers for Potentiation of Antibiotic Efficacy against Drug-Resistant Bacteria
Zeroug-Metz L, Shehu K, Bassil J, Podlecki J, Sonntag P, Koch M, Christoulaki A, Buhler E, Hirsch A, Kraegeloh A, Schneider M, Lee S (2026)
Biomacromolecules 27 (3): 1949-1968DOI: 10.1021/acs.biomac.5c02130
A multivalent TAT-arginine-biodynamer conjugate targeting the bacterial cell envelope via specific membrane interactions
Kamal M, Metwally W, Bassil J, Niebuur B, Kraus T, Herrmann J, Koch M, Hirsch A, Loretz B, Lee S, Lehr C (2026)
Biomedicine & pharmacotherapy = Biomedecine & pharmacotherapie 198DOI: 10.1016/j.biopha.2026.119304
Genome Mining Guided Identification of the Metallophore Delftichelin A from Delftia deserti
Kruijff M, Hiller L, Birkelbach J, Decker T, Götze S, Kochems R, Müller R, Hirsch A, Beemelmanns C (2026)
Journal of natural productsDOI: 10.1021/acs.jnatprod.6c00213
Identification of Natural-Product Inhibitors of the 2 C -Methyl- d -erythritol 4-Phosphate Pathway
Diamanti E, Alhayek A, Lacour A, Shahrour M, Willocx D, Illarionov B, Fischer M, Stadler M, Reiling N, Herrmann J, Müller R, Hirsch A (2026)
ACS Med. Chem. Lett.DOI: 10.1021/acsmedchemlett.6c00054
Design and Optimization of Simplified Inhibitors Targeting E. coli and K. pneumoniae IspE
Walsh D, Hamid R, Giele T, Rottmann M, Hirsch A, Hamed M, Reiling N (2026)
RSC Med. Chem.DOI: 10.1039/D5MD00874C
2025
Toward Anti-Herpesviral PROTACs: Assessing the Challenges for Targeted Protein Degradation on the Example of Kaposi's Sarcoma-Associated Herpesvirus Latency-Associated Nuclear Antigen
Berwanger A, Stein S, Brandner S, Kany A, Heinz S, Loretz B, Lehr C, Hirsch A, Lermyte F, Schulz T, Empting* M (2025)
ChemMedChemDOI: 10.1002/cmdc.202500758
Design, Synthesis, and Biological Evaluation of Mono- and Diamino-Substituted Squaramide Derivatives as Potent Inhibitors of Mycobacterial Adenosine Triphosphate (ATP) Synthase
Palme P, Grover S, Abdelaziz R, Mann L, Kany A, Ouologuem L, Bartel K, Sonnenkalb L, Reiling N, Hirsch A, …, Imming P, Richter A (2025)
J. Med. Chem. 68 (23): 25274-25289DOI: 10.1021/acs.jmedchem.5c02284
Fragment Based Drug Discovery by Microscale Thermophoresis Targeting Klebsiella pneumoniae and Escherichia coli IspE
Walsh D, Willocx D, Hamid R, Hamed M, Hirsch A (2025)
Drug design, development and therapy 19: 11345-11353DOI: 10.2147/DDDT.S538771
The One-Step Synthesis of Biologically Active Isochromans from Lignin-Derived Aromatic Monomers in Tunable Deep Eutectic Solvents
Kottayi A, Afanasenko A, Castillo-Garcia A, Elgaher W, Haupenthal J, Hirsch A, Barta K (2025)
Chem. Eur. J.DOI: 10.1002/chem.202502769
Lignin-derived guaiacols as platform chemicals for the modular synthesis of 1,2,3,4-tetrahydroquinolines and benzomorpholines
Castillo-Garcia A, Haupenthal J, Hirsch A, Barta K (2025)
RSC sustainability 3 (9): 4039-4048DOI: 10.1039/d5su00151j
Modular synthetic routes to biologically active indoles from lignin
Castillo-Garcia A, Haupenthal J, Hirsch A, Barta K (2025)
Green Chem. 27 (25): 7506-7512DOI: 10.1039/d5gc01003a
Direct monitoring of intracellular polymer degradation via BODIPY dynamic dequenching
Bassil J, Kamal M, Gabelmann A, Christoulaki A, Koch M, Hamed M, Loretz B, Gallei M, Buhler E, Lehr C, Hirsch A, Lee S (2025)
Mater. Des. 256DOI: 10.1016/j.matdes.2025.114240
Tobramycin crosslinking improves the colloidal stability of arginine chitosan biodynamers for safe and efficient siRNA delivery
Liu Y, Biesel A, Kamal M, Latta L, Loretz B, Hirsch A, Lee S, Lehr C (2025)
Int. J. Biol. Macromol. 311 (Pt 1)DOI: 10.1016/j.ijbiomac.2025.143420
1-Deoxy-D-xylulose 5-phosphate synthase: structural perspectives on an essential enzyme in isoprenoid biosynthesis
Gawriljuk V, Oerlemans R, Reddem E, Gierse R, Hirsch A, Groves M (2025)
J. Struct. Biol. 217 (3)DOI: 10.1016/j.jsb.2025.108236
Targeting isoprenoid-precursor biosynthesis in Klebsiella pneumoniae: Design, synthesis and evaluation of 1-deoxy-D-xylulose 5-phosphate synthase (DXPS) inhibitors
Eisa S, Lacour A, Johannsen S, Hamid R, Raj P, Heinz D, Hamed M, Diamanti E, Hirsch A (2025)
Bioorg. Chem. 164DOI: 10.1016/j.bioorg.2025.108877
Role of Electrostatics in Metal–Organic Junctions on Surfaces: para -Hexaphenyl-dicarbonitrile on Au(111)
Pérez Paz A, Mowbray D, Gottardi S, Solianyk L, Li J, Monjas L, Hirsch A, Stöhr M, Moreno-López J (2025)
Chem. Mater. 37 (18): 7115-7124DOI: 10.1021/acs.chemmater.5c01172
A Novel Antimalarial Agent that Inhibits Protein Synthesis in Plasmodium falciparum
Bravo P, Diamanti E, Hamed M, Bizzarri L, Wiedemar N, Passecker A, Brancucci N, Albisetti A, Gumpp C, Illarionov B, …, Rottmann M, Hirsch A (2025)
Angew. Chem. Int. Ed. (64)DOI: 10.1002/anie.202514085
Innovative zinc-binding inhibitors of Legionella pneumophila ProA reduce collagen and flagellin degradation, TLR5 evasion, and human lung tissue inflammation
Scheithauer L, Ornago C, Selmar J, Schütz C, Bianchi G, Kiefer A, Haupenthal J, Dellmann A, Huynh D, Zhang R, …, Hirsch A, Steinert M (2025)
European journal of medicinal chemistry 296DOI: 10.1016/j.ejmech.2025.117832
Domain adaptable language modeling of chemical compounds identifies potent pathoblockers for Pseudomonas aeruginosa
Kallergis G, Asgari E, Empting M, Hirsch A, Klawonn F, McHardy A (2025)
Commun. Chem. 8 (1)DOI: 10.1038/s42004-025-01484-4
Tailored phenyl ureas eradicate drug-resistant Mycobacterium tuberculosis by targeting mycolic acid cell wall assembly
Mostert D, Braun J, Zimmerman M, Engelhart C, Berndl S, Quoika P, Kany A, Proietto J, Penalva-Lopez S, Wallach J, …, Dartois V, Sieber S (2025)
Chem. Sci.DOI: 10.1039/d5sc02565f
Positive Charge in an Antimalarial Compound Unlocks Broad-Spectrum Antibacterial Activity
Braun-Cornejo M, Platteschorre M, Vries V, Bravo P, Sonawane V, Hamed M, Haupenthal J, Reiling N, Rottmann M, Piet D, …, Diamanti E, Hirsch A (2025)
JACS Au 5 (3): 1146-1156DOI: 10.1021/jacsau.4c00935
From Dyrk1A inhibitors to a novel class of antiviral agents: Targeting Enterovirus EV-A71 with 2-aryl-substituted thiophene scaffolds
Keddis P, My Tu T, Scherer H, Kany A, Hafez D, Darwish S, Abadi A, Hirsch A, Engel M, Hamed M, Horng J, Abdel-Halim M (2025)
Eur. J. Med. Chem. 287DOI: 10.1016/j.ejmech.2025.117348
Dipeptidic Phosphonates: Potent Inhibitors of Pseudomonas aeruginosa Elastase B Showing Efficacy in a Murine Keratitis Model
Kiefer A, Schütz C, Englisch C, Kolling D, Speicher S, Kany A, Shafiei R, Wadood N, Aljohmani A, Wirschem N, …, Haupenthal J, Hirsch A (2025)
Adv. Sci.DOI: 10.1002/advs.202411807
Unlocking the Antiviral Arsenal: Structure-Guided Optimization of Small-Molecule Inhibitors against RSV and hCoV-229E
Karhan C, Sake S, Gunesch A, Grethe C, Hellwinkel B, Köhler N, Kiefer A, Hapko U, Kany A, Pietschmann T, Hirsch A (2025)
European journal of medicinal chemistryDOI: 10.1016/j.ejmech.2025.117282
Targeting IspD for Anti-infective and Herbicide Development: Exploring Its Role, Mechanism, and Structural Insights
Willocx D, Diamanti E, Hirsch A (2025)
Journal of medicinal chemistryDOI: 10.1021/acs.jmedchem.4c01146
Apo structure of Mycobacterium tuberculosis 1-deoxy-d-xylulose 5-phosphate synthase DXPS: Dynamics and implications for inhibitor design
Gawriljuk V, Alhayek A, Hirsch A, Groves M (2025)
Biochemical and Biophysical Research Communications 747DOI: 10.1016/j.bbrc.2024.151246
2024
Behavioral and electrophysiological responses of the male medfly, Ceratitis capitata, to thymol and carvacrol ethers
Tabanca N, Cloonan K, Nesterkina M, Gill M, Montgomery W, Kravchenko I, Kendra P (2024)
Pest management scienceDOI: 10.1002/ps.8324
Synthesis and Structure of a Coordination Polymer of Ni(II) with 2-(4-Bromophenoxy)acetohydrazide
Martsynko ?, Nesterkina M, Finik ?, Tsymbaliuk K, Dyakonenko V, Shishkina S, Kravchenko I (2024)
Molbank 2024 (2)DOI: 10.3390/M1819
Isocyanides inhibit bacterial pathogens by covalent targeting of essential metabolic enzymes
Geißler A, Junca H, Kany A, Daumann L, Hirsch A, Pieper D, Sieber S (2024)
Chem. Sci. 15 (30): 11946-11955DOI: 10.1039/D4SC01940G
Clean Synthetic Strategies to Biologically Active Molecules from Lignin: A Green Path to Drug Discovery**
Afanasenko A, Wu X, Santi A, Elgaher W, Kany A, Shafiei R, Schulze M, Schulz T, Haupenthal J, Hirsch A, Barta K (2024)
Angewandte Chemie (Weinheim an der Bergstrasse, Germany) 136 (4)DOI: 10.1002/ange.202308131
Development of Fragment-Based Inhibitors of the Bacterial Deacetylase LpxC with Low Nanomolar Activity
Mielniczuk S, Hoff K, Baselious F, Li Y, Haupenthal J, Kany A, Riedner M, Rohde H, Rox K, Hirsch A, …, Sippl W, Holl R (2024)
Journal of medicinal chemistry 67 (19): 17363-17391DOI: 10.1021/acs.jmedchem.4c01262
Spray drying of a zinc complexing agent for inhalation therapy of pulmonary fibrosis
Stella J, Abdelaal M, Kamal M, Shehu K, Alhayek A, Haupenthal J, Hirsch A, Schneider M (2024)
European journal of pharmaceutical sciences : official journal of the European Federation for Pharmaceutical Sciences 202DOI: 10.1016/j.ejps.2024.106891
Fragment Discovery by X-Ray Crystallographic Screening Targeting the CTP Binding Site of Pseudomonas Aeruginosa IspD
Willocx D, D'Auria L, Walsh D, Scherer H, Alhayek A, Hamed M, Borel F, Diamanti E, Hirsch A (2024)
Angew. Chem., Int. Ed. Engl.DOI: 10.1002/anie.202414615
IspE kinase as an anti-infective target: Role of a hydrophobic pocket in inhibitor binding
Hamid R, Walsh D, Diamanti E, Aguilar D, Lacour A, Hamed M, Hirsch A (2024)
Structure (London, England : 1993) 32 (12): 2390-2398DOI: 10.1016/j.str.2024.10.009
Targeting the Plasmodium falciparum IspE Enzyme
Diamanti E, Steinbach A, Carvalho L, Ropponen H, Lacour A, Hamid R, Eisa S, Bravo P, Bousis S, Illarionov B, …, Sieber S, Hirsch A (2024)
ACS omega 9 (44): 44465-44473DOI: 10.1021/acsomega.4c06038
Expression and characterization of pantothenate energy-coupling factor transporters as an anti-infective drug target
Shams A, Bousis S, Diamanti E, Elgaher W, Zeimetz L, Haupenthal J, slotboom d, Hirsch A (2024)
Protein Sci. 33 (11)DOI: 10.1002/pro.5195
Studying Target-Engagement of Anti-Infectives by Solvent-Induced Protein Precipitation and Quantitative Mass Spectrometry
Bizzarri L, Steinbrunn D, Quennesson T, Lacour A, Bianchino G, Bravo P, Chaignon P, Lohse J, Mäser P, Seemann M, …, Hirsch A, Hahne H (2024)
ACS Infect. Dis. 10 (12): 4087-4102DOI: 10.1021/acsinfecdis.4c00417
Integral Solvent-Induced Protein Precipitation for Target-Engagement Studies in Plasmodium falciparum
Bravo P, Bizzarri L, Steinbrunn D, Lohse J, Hirsch A, Mäser P, Rottmann M, Hahne H (2024)
ACS Infect. Dis. 10 (12): 4073-4086DOI: 10.1021/acsinfecdis.4c00418
Dynamic Combinatorial Chemistry Unveils Nsp10 Inhibitors with Antiviral Potential Against SARS-CoV-2
Jumde R, Jézéquel G, Saramago M, Frank N, Adam S, Cunha M, Bader C, Gunesch A, Köhler N, Johannsen S, …, Arraiano C, Hirsch A (2024)
Chem. - Eur. J.DOI: 10.1002/chem.202403390
Targeting Plasmodium falciparum IspD in the Methyl-d-erythritol Phosphate Pathway: Urea-Based Compounds with Nanomolar Potency on Target and Low-Micromolar Whole-Cell Activity
Willocx D, Bizzarri L, Alhayek A, Kannan D, Bravo P, Illarionov B, Rox K, Lohse J, Fischer M, Kany A, …, Diamanti E, Hirsch A (2024)
Journal of medicinal chemistry 67 (19): 17070-17086DOI: 10.1021/acs.jmedchem.4c00212
Biodynamer Nano-Complexes and -Emulsions for Peptide and Protein Drug Delivery
Liu Y, Hamm T, Eichinger T, Kamm W, Wieland H, Loretz B, Hirsch A, Lee S, Lehr C (2024)
Int. J. Nanomedicine 19: 4429-4449DOI: 10.2147/IJN.S448578
Identification of inhibitors targeting the energy-coupling factor (ECF) transporters
Diamanti E, Souza P, Setyawati I, Bousis S, Monjas L, Swier L, Shams A, Tsarenko A, Stanek W, Jäger M, …, slotboom d, Hirsch A (2024)
Communications Biology 7 (1)DOI: 10.1038/s42003-024-05770-0
Target-Directed Dynamic Combinatorial Chemistry Affords Binders of Mycobacterium tuberculosis IspE
Braun-Cornejo M, Ornago C, Sonawane V, Haupenthal J, Kany A, Diamanti E, Jézéquel G, Reiling N, Blankenfeldt W, Maas P, Hirsch A (2024)
ACS omegaDOI: 10.1021/acsomega.4c05537
Evaluation of ketoclomazone and its analogues as inhibitors of 1-deoxy-d-xylulose 5-phosphate synthases and other thiamine diphosphate (ThDP)-dependent enzymes
Chan A, Ho T, Fathoni I, Hamid R, Hirsch A, Saliba K, Leeper F (2024)
RSC Med. Chem. 15 (5): 1773-1781DOI: 10.1039/D4MD00083H
Two natural compounds as potential inhibitors against the Helicobacter pylori and Acinetobacter baumannii IspD enzymes
Chen X, Zhao H, Wang C, Hamed M, Shang Q, Yang Y, Diao X, Sun X, Hu W, Jiang X, …, Wu D, Zhuang J (2024)
Int. J. Antimicrob. Agents 63 (5)DOI: 10.1016/j.ijantimicag.2024.107160
Arg-biodynamers as antibiotic potentiators through interacting with Gram-negative outer membrane lipopolysaccharides
Kamal M, Bassil J, Loretz B, Hirsch A, Lee S, Lehr C (2024)
Eur J Pharm Biopharm 200DOI: 10.1016/j.ejpb.2024.114336
AI is a viable alternative to high throughput screening: a 318-target study
Wallach I, Hirsch, Anna K. H. et al. (2024)
Sci. Rep. 14 (1)DOI: 10.1038/s41598-024-54655-z
Cryo-EM structure of 1-deoxy-D-xylulose 5-phosphate synthase DXPS from Plasmodium falciparum reveals a distinct N-terminal domain
Gawriljuk V, Godoy A, Oerlemans R, Welker L, Hirsch A, Groves M (2024)
Nat. Commun. 15 (1)DOI: 10.1038/s41467-024-50671-9
Dual inhibitors of Pseudomonas aeruginosa virulence factors LecA and LasB
Metelkina O, Konstantinovic J, Klein A, Shafiei R, Fares M, Alhayek A, Yahiaoui S, Elgaher W, Haupenthal J, Titz* A, Hirsch* A (2024)
Chem. Sci. 15DOI: 10.1039/D4SC02703E
Discovery and optimization of thiazole-based quorum sensing inhibitors as potent blockers of Pseudomonas aeruginosa pathogenicity
Abdelsamie A, Hamed M, Schütz C, Röhrig T, Kany A, Schmelz S, Blankenfeldt W, Hirsch A, Hartmann R, Empting M (2024)
Eur. J. Med. Chem. 276DOI: 10.1016/j.ejmech.2024.116685
Thermotropic liquid crystals in drug delivery: A versatile carrier for controlled release
Nesterkina M, Kravchenko* I, Hirsch A, Lehr C (2024)
Eur. J. Pharm. Biopharm. 200DOI: 10.1016/j.ejpb.2024.114343
Target repurposing unravels avermectins and derivatives as novel antibiotics inhibiting energy-coupling factor transporters (ECFTs)
Haupenthal J, Rafehi M, Kany A, Lespine A, Stefan K, Hirsch* A, Stefan* S (2024)
Arch. Pharm.DOI: 10.1002/ardp.202400267
Point mutations in the ygiV promoter region lead to cystobactamid resistance and reduced virulence in E. coli
Müller R, Risch T, Kolling D, Mostert D, Seedorf T, Heimann D, Kohnhäuser D, Deschner F, Fries F, Solga D, …, Herrmann J, Sieber S (2024)
BookDOI: 10.21203/rs.3.rs-3751821/v1
Novel 6-hydroxybenzothiazol-2-carboxamides as potent and selective monoamine oxidase B inhibitors endowed with neuroprotective activity
Al-Saad O, Gabr M, Darwish S, Rullo M, Pisani L, Miniero D, Liuzzi G, Kany A, Hirsch A, Abadi A, …, Catto M, Abdel-Halim M (2024)
European journal of medicinal chemistryDOI: 10.1016/j.ejmech.2024.116266
Drug repurposing screen identifies lonafarnib as respiratory syncytial virus fusion protein inhibitor
Sake S, Zhang X, Rajak M, Urbanek-Quaing M, Carpentier A, Gunesch A, Grethe C, Matthaei A, Rückert J, Galloux M, …, Haid* S, Pietschmann* T (2024)
Nat. Commun. 15 (1)DOI: 10.1038/s41467-024-45241-y
High Target Homology Does Not Guarantee Inhibition: Aminothiazoles Emerge as Inhibitors of Plasmodium falciparum
Johannsen S, Gierse R, Krüger A, Edwards R, Nanna V, Fontana A, Di Zhu, Masini T, Carvalho L, Poizat M, …, Wrenger C, Hirsch* A (2024)
ACS Infect. Dis.DOI: 10.1021/acsinfecdis.3c00670
Hit optimization by dynamic combinatorial chemistry on Streptococcus pneumoniae energy-coupling factor transporter ECF-PanT
Exapicheidou I, Shams A, Ibrahim H, Tsarenko A, Backenköhler M, Hamed M, Diamanti E, Volkamer A, slotboom d, Hirsch A (2024)
Chem. Commun. 60 (7): 870-873DOI: 10.1039/D3CC04738E
Development and evaluation of 2,4-disubstituted-5-aryl pyrimidine derivatives as antibacterial agents
Khalifa H, Rasheed S, Haupenthal J, Herrmann J, Mandour Y, Abadi A, Engel M, Müller R, Hirsch A, Abdel-Halim* M, Hamed* M (2024)
Archiv der PharmazieDOI: 10.1002/ardp.202300656
2023
Inhibitors of the Elastase LasB for the Treatment of Pseudomonas aeruginosa Lung Infections
Konstantinovic J, Kany A, Alhayek A, Abdelsamie A, Sikandar A, Voos K, Yao Y, Andreas A, Shafiei R, Loretz B, …, Haupenthal J, Hirsch A (2023)
ACS Cent. Sci. 9 (12): 2205-2215DOI: 10.1021/acscentsci.3c01102
Clean Synthetic Strategies to Biologically Active Molecules from Lignin: A Green Path to Drug Discovery
Afanasenko A, Wu X, Santi A, Elgaher W, Kany A, Shafiei R, Schulze M, Schulz T, Haupenthal J, Hirsch A, Barta K (2023)
Angew. Chem. Int. Ed.DOI: 10.1002/anie.202308131
Identification of HuR–RNA Interfering Compounds by Dynamic Combinatorial Chemistry and Fluorescence Polarization
Della Volpe S, Listro R, Ambrosio F, Garbagnoli M, Linciano P, Rossi D, Costa G, Alcaro S, Vasile F, Hirsch A, Collina S (2023)
ACS Med. Chem. Lett.DOI: 10.1021/acsmedchemlett.3c00303
1-deoxy-D-xylulose-5-phosphate synthase from Pseudomonas aeruginosa and Klebsiella pneumoniae reveals conformational changes upon cofactor binding
Hamid R, Adam S, Lacour A, Monjas L, Köhnke J, Hirsch A (2023)
The Journal of biological chemistryDOI: 10.1016/j.jbc.2023.105152
NRF2 activators inhibit influenza A virus replication by interfering with nucleo-cytoplasmic export of viral RNPs in an NRF2-independent manner
Waqas F, Shehata M, Elgaher W, Lacour A, Kurmasheva N, Begnini F, Kiib A, Dahlmann J, Chen C, Pavlou A, …, Pleschka S, Pessler F (2023)
PLOS Pathogens 19 (7)DOI: 10.1371/journal.ppat.1011506
pH-Responsive Dynaplexes as Potent Apoptosis Inductors by Intracellular Delivery of Survivin siRNA
Liu Y, Ashmawy S, Latta L, Weiss A, Kiefer A, Nasr S, Loretz B, Hirsch A, Lee S, Lehr C (2023)
Biomacromolecules 24 (8): 3742-3754DOI: 10.1021/acs.biomac.3c00424
Exploring the Translational Gap of a Novel Class of Escherichia coli IspE Inhibitors
Ropponen H, Diamanti E, Johannsen S, Illarionov B, Hamid R, Jaki M, Sass P, Fischer M, Haupenthal J, Hirsch A (2023)
ChemMedChemDOI: 10.1002/cmdc.202300346
Artificial intelligence for natural product drug discovery
Mullowney M, Duncan K, Elsayed S, Garg N, van der Hooft J, Martin N, Meijer D, Terlouw B, Biermann F, Blin K, …, Robinson S, Medema M (2023)
Nat Rev Drug DiscovDOI: 10.1038/s41573-023-00774-7
Thermoresponsive cholesteric liquid-crystal systems doped with terpenoids as drug delivery systems for skin applications
Nesterkina M, Vashchenko O, Vashchenko P, Lisetski L, Kravchenko I, Hirsch A, Lehr C (2023)
European journal of pharmaceutics and biopharmaceutics : official journal of Arbeitsgemeinschaft fur Pharmazeutische Verfahrenstechnik e.VDOI: 10.1016/j.ejpb.2023.09.002
Selective Activation of TRPC6 Ion Channel by Metallated Type-B Polyprenylated Polycyclic Acylphloroglucinols
Peslalz P, Kraus F, Izzo F, Bleisch A, El Hamdaoui Y, Schulz I, Kany A, Hirsch A, Friedland K, Plietker B (2023)
ManuscriptDOI: 10.26434/chemrxiv-2023-6w94r
Design of thiamine analogues for inhibition of thiamine diphosphate (ThDP)-dependent enzymes: Systematic investigation through Scaffold-Hopping and C2-Functionalisation
Chan A, Ho T, Irfan R, Hamid R, Rudge E, Iqbal A, Turner A, Hirsch A., Leeper F (2023)
Bioorganic chemistry 138DOI: 10.1016/j.bioorg.2023.106602
Facile Production of the Pseudomonas aeruginosa Virulence Factor LasB in E. coli for Structure-Based Drug Design
Kolling D, Haupenthal J, Hirsch A, Köhnke J (2023)
ChemBioChemDOI: 10.1002/cbic.202300185
Structure of Mycobacterium tuberculosis 1-Deoxy-D-Xylulose 5-Phosphate Synthase in Complex with Butylacetylphosphonate
Gawriljuk V, Oerlemans R, Gierse R, Jotwani R, Hirsch A, Groves M (2023)
Crystals 13 (5)DOI: 10.3390/cryst13050737
Not Every Hit-Identification Technique Works on 1-Deoxy-d-Xylulose 5-Phosphate Synthase (DXPS): Making the Most of a Virtual Screening Campaign
Johannsen S, Gierse R, Olshanova A, Smerznak E, Laggner C, Eschweiler L, Adeli Z, Hamid R, Alhayek A, Reiling N, Haupenthal J, Hirsch A (2023)
ChemMedChemDOI: 10.1002/cmdc.202200590
Genotoxic and mutational potential of monocyclic terpenoids (carvacrol, carvone and thymol) in Drosophila melanogaster
Nesterkina M, Bilokon S, Alieksieieva T, Kravchenko I, Hirsch A (2023)
Toxicol. Rep. 10DOI: 10.1016/j.toxrep.2023.02.009
Fighting antibiotic resistance-strategies and (pre)clinical developments to find new antibacterials
Walesch S, Birkelbach J, Jézéquel G, Haeckl F, Hegemann J, Hesterkamp T, Hirsch A, Hammann P, Müller R (2023)
EMBO reports 24 (1)DOI: 10.15252/embr.202256033
Towards Translation of PqsR Inverse Agonists: From In Vitro Efficacy Optimization to In Vivo Proof-of-Principle
Hamed M, Abdelsamie A, Rox K, Schütz C, Kany A, Röhrig T, Schmelz S, Blankenfeldt W, Arce-Rodriguez A, Borrero-de Acuña J, …, Hartmann R, Empting M (2023)
Adv. Sci. (Online)DOI: 10.1002/advs.202204443
2022
PHARMACOLOGICAL AND PHYSICO-CHEMICAL PROPERTIES OF COMPOSITIONS BASED ON BIOSURFACTANTS AND N-CONTAINING HETEROCYCLIC DERIVATIVES OF 1,4-NAPHTHOQUINONE
Polish N, Nesterkina M, Karkhut A, Marintsova N, Zhurakhivska L, Volianiuk K, Pokynbroda T, Kravchenko I, Karpenko E (2022)
J microb biotech food sci 12 (3)DOI: 10.55251/jmbfs.5956
(1 R ,2 S ,5 R )-5-Methyl-2-(propan-2-yl)cyclohexyl 4-amino-3-phenylbutanoate hydrochloride: Synthesis and anticonvulsant activity
Nesterkina M, Musatov V, Honcharova O, Kravchenko I (2022)
Open Chemistry 20 (1): 703-707DOI: 10.1515/chem-2022-0189
New Ketene Dithioacetals Generated from 2-Nitroperchlorobutadiene and Investigation of Their Antibacterial, Antifungal, Anticonvulsant and Antidepressant Activities
Aydinli S, Bulut E, Deniz N, Sayil C, Komarovska-Porokhnyavets O, Lubenets V, Zvarych V, Stasevych M, Nesterkina M, Kravchenko I (2022)
Chemistry & Biodiversity 19 (7)DOI: 10.1002/cbdv.202100931
Discovery of the First Selective Nanomolar Inhibitors of ERAP2 by Kinetic Target‐Guided Synthesis
Camberlein V, Fléau C, Sierocki P, Li L, Gealageas R, Bosc D, Guillaume V, Warenghem S, Leroux F, Rosell M, …, Bouvier M, Deprez-Poulain R (2022)
Angew. Chemie 134 (39)DOI: 10.1002/ange.202203560
Synthesis, biological evaluation, and molecular docking studies of aldotetronic acid-based LpxC inhibitors
Wimmer S, Hoff K, Martin B, Grewer M, Denni L, Lascorz Massanet R, Raimondi M, Bülbül E, Melesina J, Hotop S, …, Sippl W, Holl R (2022)
Bioorganic chemistry 131DOI: 10.1016/j.bioorg.2022.106331
Proteoid biodynamers for safe mRNA transfection via pH-responsive nanorods enabling endosomal escape
Lee S, Nasr S, Rasheed S, Liu Y, Hartwig O, Kaya C, Boese A, Koch M, Herrmann J, Müller R, …, Hirsch A, Lehr C (2022)
Journal of controlled release : official journal of the Controlled Release Society 353: 915-929DOI: 10.1016/j.jconrel.2022.12.018
Baicalin lipid nanocapsules for treatment of glioma: characterization, mechanistic cytotoxicity, and pharmacokinetic evaluation
Ibrahim A, Abdel Gaber S, Fawzi Kabil M, Ahmed-Farid O, Hirsch A, El-Sherbiny I, Nasr M (2022)
Expert Opin. Drug Deliv. 19 (11): 1549-1560DOI: 10.1080/17425247.2022.2139370
Introduction to themed collection on fragment-based drug discovery
Rees D, Hirsch A, Erlanson D (2022)
RSC Med. Chem. 13DOI: 10.1039/D2MD90037H
An Efficient Way to Screen Inhibitors of Energy-Coupling Factor (ECF) Transporters in a Bacterial Uptake Assay
Bousis S, Winkler S, Haupenthal J, Fulco F, Diamanti E, Hirsch A (2022)
International journal of molecular sciences 23 (5)DOI: 10.3390/ijms23052637
Respiratory Syncytial Virus Two-Step Infection Screen Reveals Inhibitors of Early and Late Life Cycle Stages
Sake S, Kosch C, Blockus S, Haid S, Gunesch A, Zhang X, Friesland M, Trummer S, Grethe C, Kühnel A, …, Schulz T, Pietschmann T (2022)
Antimicrobial agents and chemotherapyDOI: 10.1128/aac.01032-22
Discovery and Characterization of Synthesized and FDA-Approved Inhibitors of Clostridial and Bacillary Collagenases
Alhayek A, Abdelsamie A, Schönauer E, Camberlein V, Hutterer E, Posselt G, Serwanja J, Blöchl C, Huber C, Haupenthal J, …, Wessler S, Hirsch A (2022)
Journal of medicinal chemistry 65 (19): 12933-12955DOI: 10.1021/acs.jmedchem.2c00785
Discovery of novel drug-like antitubercular hits targeting the MEP pathway enzyme DXPS by strategic application of ligand-based virtual screening
Di Zhu, Johannsen S, Masini T, Simonin C, Haupenthal J, Illarionov B, Andreas A, Awale M, Gierse R, van der Laan T, …, Reymond J, Hirsch A (2022)
Chem. Sci. 13 (36): 10686-10698DOI: 10.1039/D2SC02371G
Screening of Natural Products and Small Molecules Uncovers Novel Coronavirus 1a/1b Frameshifting Inhibitors with Antiviral Properties
Kibe A, Elgaher W, Rand U, Zimmer M, Kany A, Hermann J, Müller R, Cicin-Sain L, Hirsch A, Caliskan N (2022)
SSRN JournalDOI: 10.2139/ssrn.4157446
Design, Synthesis, Antimicrobial Activity, and Molecular Docking of Some New Diclofenac Derivatives
Tolba M, Hamed M, Sayed M, Kamal El-Dean A, Abdel-Mohsen S, Ibrahim O, Elgaher W, Hirsch A, Saddik A (2022)
Polycyclic Aromatic Compounds: 1-16DOI: 10.1080/10406638.2022.2102661
Structural analysis of 1-deoxy-D-xylulose 5-phosphate synthase from Pseudomonas aeruginosa and Klebsiella pneumoniae reveals conformational changes upon cofactor binding
Hamid R, Adam S, Lacour A, Gomez L, Hirsch A (2022)
bioRxivDOI: 10.1101/2022.07.04.498669
Identification of RAD51-BRCA2 Inhibitors Using N-Acylhydrazone-Based Dynamic Combinatorial Chemistry
Bagnolini G, Balboni B, Schipani F, Gioia D, Veronesi M, Franco F, Kaya C, Jumde R, Ortega J, Girotto S, …, Roberti M, Cavalli A (2022)
ACS Med. Chem. Lett. 13 (8): 1262-1269DOI: 10.1021/acsmedchemlett.2c00063
The Structures and Binding Modes of Small-Molecule Inhibitors of Pseudomonas aeruginosa Elastase LasB
Camberlein V, Jézéquel G, Haupenthal J, Hirsch A (2022)
Antibiotics 11 (8)DOI: 10.3390/antibiotics11081060
Transferring Microclusters of P. aeruginosa Biofilms to the Air-Liquid Interface of Bronchial Epithelial Cells for Repeated Deposition of Aerosolized Tobramycin
Horstmann J, Laric A, Boese A, Yildiz D, Röhrig T, Empting M, Frank N, Krug D, Müller R, Schneider-Daum N, Souza Carvalho-Wodarz C, Lehr C (2022)
ACS infectious diseases 8 (1): 137-149DOI: 10.1021/acsinfecdis.1c00444
Structure-Guided Optimization of Small-Molecule Folate Uptake Inhibitors Targeting the Energy-Coupling Factor Transporters
Kiefer A, Bousis S, Hamed M, Diamanti E, Haupenthal J, Hirsch A (2022)
J. Med. Chem.DOI: 10.1021/acs.jmedchem.1c02114
Citraconate inhibits ACOD1 (IRG1) catalysis, reduces interferon responses and oxidative stress, and modulates inflammation and cell metabolism
Chen F, Elgaher W, Winterhoff M, Büssow K, Waqas F, Graner E, Pires-Afonso Y, Casares Perez L, La Vega L, Sahini N, …, Hirsch A, Pessler F (2022)
Nature metabolism 4 (5): 534-546DOI: 10.1038/s42255-022-00577-x
Targeting Extracellular Bacterial Proteases for the Development of Novel Antivirulence Agents
Kaya C, Hirsch A (2022)
Chimia 76 (5)DOI: 10.2533/chimia.2022.402
Design and Synthesis of Novel Bis-Imidazolyl Phenyl Butadiyne Derivatives as HCV NS5A Inhibitors
Hamdy J, Emadeldin N, Hamed M, Frakolaki E, Katsamakas S, Vassilaki N, Zoidis G, Hirsch A, Abdel-Halim M, Abadi A (2022)
Pharmaceuticals 15 (5)DOI: 10.3390/ph15050632
First crystal structures of 1-deoxy-D-xylulose 5-phosphate synthase (DXPS) from Mycobacterium tuberculosis indicate a distinct mechanism of intermediate stabilization
Gierse R, Oerlemans R, Reddem E, Gawriljuk V, Alhayek A, Baitinger D, Jakobi H, Laber B, Lange G, Hirsch A, Groves M (2022)
Sci. Rep. 12 (1)DOI: 10.1038/s41598-022-11205-9
N-Aryl-2-iso-butylmercaptoacetamides: the discovery of highly potent and selective inhibitors of Pseudomonas aeruginosa virulence factor LasB and Clostridium histolyticum virulence factor ColH
Voos K, Yahiaoui S, Konstantinovic J, Schönauer E, Alhayek A, Sikandar A, Si Chaib K, Ramspoth T, Rox K, Haupenthal J, …, Ducho C, Hirsch A (2022)
ChemRxivDOI: 10.26434/chemrxiv-2022-fjrqr
Structure-Based Design of α-Substituted Mercaptoacetamides as Inhibitors of the Virulence Factor LasB from Pseudomonas aeruginosa
Kaya C, Walter I, Alhayek A, Shafiei R, Jézéquel G, Andreas A, Konstantinovic J, Schönauer E, Sikandar A, Haupenthal J, …, Hartmann R, Hirsch A (2022)
ACS Infect. Dis.DOI: 10.1021/acsinfecdis.1c00628
N-Aryl Mercaptopropionamides as Broad-Spectrum Inhibitors of Metallo-β-Lactamases
Kaya C, Konstantinovic J, Kany A, Andreas A, Kramer J, Brunst S, Weizel L, Rotter M, Frank D, Yahiaoui S, …, Wichelhaus T, Hirsch A (2022)
Journal of medicinal chemistry 65 (5): 3913-3922DOI: 10.1021/acs.jmedchem.1c01755
Metabolic profiling of S-praziquantel: Structure elucidation using the crystalline sponge method in combination with mass spectrometry and nuclear magnetic resonance
Rosenberger L, Jenniches J, Essen C, Khutia A, Kühn C, Marx A, Georgi K, Hirsch A, Hartmann R, Badolo L (2022)
Drug metabolism and disposition: the biological fate of chemicalsDOI: 10.1124/dmd.121.000663
Inhibition of Collagenase Q1 of Bacillus cereus as a Novel Antivirulence Strategy for the Treatment of Skin‐Wound Infections
Alhayek A, Khan E, Schönauer E, Däinghaus T, Shafiei R, Voos K, Han M, Ducho C, Posselt G, Wessler S, …, del Campo A, Hirsch A (2022)
Adv. Therap.DOI: 10.1002/adtp.202100222
Bacteriomimetic Liposomes Improve Antibiotic Activity of a Novel Energy-Coupling Factor Transporter Inhibitor
Drost M, Diamanti E, Fuhrmann K, Goes A, Shams A, Haupenthal J, Koch M, Hirsch A, Fuhrmann G (2022)
Pharmaceutics 14 (1)DOI: 10.3390/pharmaceutics14010004
2021
Synthesis and pharmacological evaluation of novel naphthoquinone derivatives containing 1,2,4-triazine and 1,2,4-triazole moieties of methylene blue on the surface of a "core–shell" type catalyst for the Fenton system
Polish N, Nesterkina M, Protunkevych M, Karkhut A, Marintsova N, Polovkovych S, IKravchenko I, Voskoboinik O, Kovalenko S, Karpenko O (2021)
Vopr. Khim. Khim. Tekhnol. (5): 97-104DOI: 10.32434/0321-4095-2021-138-5-97-104
Citatronic Acid and Derivates thereof for use as a medicament
Pessler F., Chen F., Winterhoff M., Büssow K., Blankenfeldt W., Hirsch A. K. H., Elgaher W (2021)
Patent (WO2022223778, 2022)
N-Phenyl-3-Mercaptopropanamide Derivatives as Metallo-Beta-Lactamase Inhibitors for the Treatment of Bacterial Infections
Hartmann R, Konstantinovic J, Haupenthal J, Hirsch A, Kany A, Kaya C, Yahiaoui S, Wichelhaus T, Proschak E (2021)
Patent A61K31/5375; A61P31/04; C07C233/15; C07C233/25; C07C233/33; C07C233/43; C07C233/54; C07C319/02; C07C323/52; C07D295/22; (WO2021191219A1)
New PqsR Inverse Agonist
Schütz C, Empting M, Ahmed S, Hamed M, Hartmann R, Röhrig T, Kany A, Hirsch A (2021)
Patent A61K31/4439; A61K31/506; A61P31/04; C07D401/12; C07D403/12; (WO2021136803A1)
Novel PqsR Inverse Agonists
Hamed M, Ahmed S, Empting. M., Schütz C, Hartmann R, Röhrig T, Kany A, Hirsch A (2021)
Patent A61K31/4439; A61P31/04; C07D401/14; C07D417/14; (WO2021136805A1)
Towards the sustainable discovery and development of new antibiotics
Miethke M, Pieroni M, Weber T, Brönstrup M, Hammann P, Halby L, Arimondo P, Glaser P, Aigle B, Bode H, …, Moser H, Müller R (2021)
Nature reviews. Chemistry 5 (10): 726-749DOI: 10.1038/s41570-021-00313-1
Novel (‒)-carvone derivatives as potential anticonvulsant and analgesic agents
Nesterkina M, Barbalat D, Konovalova I, Shishkina S, Atakay M, Salih B, Kravchenko I (2021)
Natural product research 35 (23): 4978-4987DOI: 10.1080/14786419.2020.1756804
Simultaneous Complexation and Microextraction Using Verbenone Hydrazone as the Ligand with Slotted Quartz Tube-Flame Atomic Absorption Spectrometry (FAAS) for the Sensitive Determination of Copper
Özzeybek G, Borahan T, Nesterkina M, Kravchenko I, Bakirdere S (2021)
Analytical letters 54 (14): 2376-2386DOI: 10.1080/00032719.2020.1866594
Quantitative structure–activity relationship study on prolonged anticonvulsant activity of terpene derivatives in pentylenetetrazole test
Nesterkina M, Muratov V, Ognichenko L, Kravchenko I, Kuz’min V (2021)
Open Chemistry 19 (1): 1184-1192DOI: 10.1515/chem-2021-0108
Rheological Properties of Hyaluronic Acid Diluted Solutions as Components of Cosmetics
Svetlana Saitarly, Yuriy Pushkarev, Nesterkina M, Serhat Öztürk, Iryna Kravchenko (2021)
Biointerface Res Appl Chem 12 (2): 1907-1915DOI: 10.33263/BRIAC122.19071915
Terpenoid Hydrazones as Biomembrane Penetration Enhancers: FT-IR Spectroscopy and Fluorescence Probe Studies
Nesterkina M, Smola S, Rusakova N, Kravchenko I (2021)
Molecules (Basel, Switzerland) 27 (1)DOI: 10.3390/molecules27010206
Targeting the IspD Enzyme in the MEP Pathway: Identification of a Novel Fragment Class
Diamanti E, Hamed M, Lacour A, Bravo P, Illarionov B, Fischer M, Rottmann M, Witschel M, Hirsch A (2021)
ChemMedChemDOI: 10.1002/cmdc.202100679
Substrate-Inspired Fragment Merging and Growing Affords Efficacious LasB Inhibitors
Kaya C, Walter I, Yahiaoui S, Sikandar A, Alhayek A, Konstantinovic J, Kany A, Haupenthal J, Köhnke J, Hartmann R, Hirsch A (2021)
Angewandte Chemie (International ed. in English)DOI: 10.1002/anie.202112295
Redesigning of the cap conformation and symmetry of the diphenylethyne core to yield highly potent pan-genotypic NS5A inhibitors with high potency and high resistance barrier
Abdallah M, Hamed M, Frakolaki E, Katsamakas S, Vassilaki N, Bartenschlager R, Zoidis G, Hirsch A, Abdel-Halim M, Abadi A (2021)
European journal of medicinal chemistryDOI: 10.1016/j.ejmech.2021.114034
Unveiling Adatoms in On-Surface Reactions: Combining Scanning Probe Microscopy with van't Hoff Plots
Moreno-López J, Pérez Paz A, Gottardi S, Solianyk L, Li J, Monjas L, Hirsch A, Mowbray D, Stöhr M (2021)
The journal of physical chemistry. C, Nanomaterials and interfaces 125 (18): 9847-9854DOI: 10.1021/acs.jpcc.1c03134
1st Spring Virtual Meeting on Medicinal Chemistry
Sousa M, Marques M, Faustino M (2021)
Chemistry Proceedings 4 (1)DOI: 10.3390/chemproc2021004001
Design, synthesis, and biological evaluation of novel benzimidazole derivatives as sphingosine kinase 1 inhibitor
Khairat S, Omar M, Ragab F, Roy S, Turab Naqvi A, Abdelsamie A, Hirsch A, Galal S, Hassan M, El Diwani H (2021)
Archiv der Pharmazie 354 (9)DOI: 10.1002/ardp.202100080
Identification of N,N-arylalkyl-picolinamide derivatives targeting the RNA-binding protein HuR, by combining biophysical fragment-screening and molecular hybridization
Della Volpe S, Linciano P, Listro R, Tumminelli E, Amadio M, Bonomo I, Elgaher W, Adam S, Hirsch A, Boeckler F, …, Rossi D, Collina S (2021)
Bioorganic chemistry 116DOI: 10.1016/j.bioorg.2021.105305
Expanding the Myxochelin Natural Product Family by Nicotinic Acid Containing Congeners
Frank N, Széles M, Akone S, Rasheed S, Hüttel S, Frewert S, Hamed M, Herrmann J, Schuler S, Hirsch A, Müller R (2021)
Molecules 26 (16)DOI: 10.3390/molecules26164929
N-Aryl mercaptoacetamides as potential multi-target inhibitors of metallo-β-lactamases (MBLs) and the virulence factor LasB from Pseudomonas aeruginosa
Yahiaoui S, Voos K, Haupenthal J, Wichelhaus T, Frank D, Weizel L, Rotter M, Brunst S, Kramer J, Proschak E, Ducho C, Hirsch A (2021)
RSC Med. Chem.DOI: 10.1039/D1MD00187F
Crystalline sponge affinity screening: A fast tool for soaking condition optimization without the need of X-ray diffraction analysis
Rosenberger L, Essen C, Khutia A, Kühn C, Georgi K, Hirsch A, Hartmann R, Badolo L (2021)
European journal of pharmaceutical sciences : official journal of the European Federation for Pharmaceutical Sciences 164DOI: 10.1016/j.ejps.2021.105884
A New PqsR Inverse Agonist Potentiates Tobramycin Efficacy to Eradicate Pseudomonas aeruginosa Biofilms
Schütz C, Ho D, Hamed M, Abdelsamie A, Röhrig T, Herr C, Kany A, Rox K, Schmelz S, Siebenbürger L, …, Lehr C, Empting M (2021)
Advanced science (Weinheim, Baden-Wurttemberg, Germany) 8 (12)DOI: 10.1002/advs.202004369
“Clicking“ fragment leads to novel dual-binding cholinesterase inhibitors
Moleda Z, Zawadzka A, Czarnocki Z, Monjas L, Hirsch A, Budzianowski A, Maurin J (2021)
Bioorg Med ChemDOI: 10.1016/j.bmc.2021.116269
Phosphonate as a Stable Zinc‐Binding Group for “Pathoblocker” Inhibitors of Clostridial Collagenase H (ColH) (ChemMedChem 8/2021)
Voos K, Schönauer E, Alhayek A, Haupenthal J, Andreas A, Müller R, Hartmann R, Brandstetter H, Hirsch A, Ducho C (2021)
ChemMedChem 16 (8): 1198-1198DOI: 10.1002/cmdc.202100229
Hit-optimization using target-directed dynamic combinatorial chemistry: Development of inhibitors of the anti-infective target 1-deoxy-D-xylulose-5-phosphate synthase
Jumde R, Guadigni M, Gierse R, Alhayek A, Di Zhu, Hamid Z, Johannsen S, Elgaher W, Neusens P, Nehls C, …, Reiling N, Hirsch A (2021)
Chemical ScienceDOI: 10.1039/D1SC00330E
Search for the Active Ingredients from a 2-Aminothiazole DMSO Stock Solution with Antimalarial Activity
Ropponen H, Bader C, Diamanti E, Illarionov B, Rottmann M, Fischer M, Witschel M, Müller R, Hirsch A (2021)
ChemMedChem 16 (13): 2089-2093DOI: 10.1002/cmdc.202100067
Mastering the Gram-Negative Bacterial Barrier - Chemical Approaches to Increase Bacterial Bioavailability of Antibiotics
Ropponen H, Richter R, Hirsch A, Lehr C (2021)
Advanced Drug Delivery ReviewsDOI: 10.1016/j.addr.2021.02.014
Assessment of the rules related to gaining activity against Gram-negative bacteria
Ropponen H, Diamanti E, Siemens A, Illarionov B, Haupenthal J, Fischer M, Rottmann M, Witschel M, Hirsch A (2021)
RSC Med. Chem.DOI: 10.1039/D0MD00409J
Enhancing glycan stability via site-selective fluorination: modulating substrate orientation by molecular design
Axer A, Jumde R, Adam S, Faust A, Schäfers M, Fobker M, Koehnke J, Hirsch A, Gilmour R (2021)
Chem. Sci. 12 (4): 1286-1294DOI: 10.1039/D0SC04297H
Identification of a 1-deoxy-D-xylulose-5-phosphate synthase (DXS) mutant with improved crystallographic properties
Gierse R, Reddem E, Alhayek A, Baitinger D, Hamid Z, Jakobi H, Laber B, Lange G, Hirsch A, Groves (2021)
Biochemical and Biophysical Research Communications 539DOI: 10.1016/j.bbrc.2020.12.069
2020
9,10-Anthraquinone Dithiocarbamates as Potential Pharmaceutical Substances with Pleiotropic Actions: Computerized Prediction of Biological Activity and Experimental Validation
Stasevich M, Zvarich V, Novikov V, Zagorodnyaya S, Povnitsa O, Chaika M, Nesterkina M, Kravchenko I, Druzhilovskii D, Poroikov V (2020)
Pharm Chem J 53 (10): 905-913DOI: 10.1007/s11094-020-02098-x
Phytochemical analysis and anti-inflammatory activity of Cladophora aegagropila extract
Aleksandrova A, Nesterkina M, Gvozdii S, Kravchenko I (2020)
J Herbmed Pharmacol 9 (1): 81-85DOI: 10.15171/jhp.2020.12
Design, synthesis and pharmacological profile of (−)-verbenone hydrazones
Nesterkina M, Barbalat D, Kravchenko I (2020)
Open Chemistry 18 (1): 943-950DOI: 10.1515/chem-2020-0103
Synthesis and Evaluation on Anticonvulsant and Antidepressant Activities of Naphthoquinone Derivatives Containing Pyrazole and Pyrimidine Fragments
Polish N, Nesterkina M, Marintsova N, Karkhut A, Kravchenko I, Novikov V, Khairulin A (2020)
ACSi 67 (3): 934-939DOI: 10.17344/acsi.2020.5938
Toxic effect and genotoxicity of carvacrol ethers in Drosophila melanogaster
Nesterkina M, Bilokon S, Alieksieieva T, Chebotar S, Kravchenko I (2020)
Mutat. Res. 821 (2)DOI: 10.1016/j.mrfmmm.2020.111713
QSAR models for analgesic activity prediction of terpenes and their derivatives
Nesterkina M, Ognichenko L, Shyrykalova A, Kravchenko I, Kuz’min V (2020)
Struct Chem 31 (3): 947-954DOI: 10.1007/s11224-019-01479-7
2-Propyl-N′-[1,7,7-trimethylbicyclo[2.2.1]hept-2-ylidene]pentanehydrazide
Nesterkina M, Barbalat D, Rakipov I, Kravchenko I (2020)
Molbank 2020 (4)DOI: 10.3390/M1164
A hydrogel-based in vitro assay for the fast prediction of antibiotic accumulation in Gram-negative bacteria
Richter R, Kamal M, García-Rivera M, Kaspar J, Junk M, Elgaher W, Srikakulam S, Gress A, Beckmann A, Grißmer A, …, Schneider-Daum N, Lehr C (2020)
Materials today. Bio 8DOI: 10.1016/j.mtbio.2020.100084
Micro-rheological properties of lung homogenates correlate with infection severity in a mouse model of Pseudomonas aeruginosa lung infection
Murgia X, Kany A, Herr C, Ho D, Rossi C, Bals R, Lehr C, Hirsch A, Hartmann R, Empting M, Röhrig T (2020)
Scientific Reports 10 (1)DOI: 10.1038/s41598-020-73459-5
Semisynthesis and biological evaluation of amidochelocardin derivatives as broad-spectrum antibiotics
Grandclaudon C, Birudukota N, Elgaher W, Jumde R, Yahiaoui S, Arisetti N, Hennessen F, Hüttel S, Stadler M, Herrmann J, …, Hirsch A, Brönstrup M (2020)
European journal of medicinal chemistry 188DOI: 10.1016/j.ejmech.2019.112005
Discovery of Small-Molecule Stabilizers of 14-3-3 Protein-Protein Interactions via Dynamic Combinatorial Chemistry
Hartman A, Elgaher W, Hertrich N, Andrei S, Ottmann C, Hirsch A (2020)
ACS medicinal chemistry letters 11 (5): 1041-1046DOI: 10.1021/acsmedchemlett.9b00541
Evaluation of Bacterial RNA Polymerase Inhibitors in a Staphylococcus aureus-Based Wound Infection Model in SKH1 Mice
Haupenthal J, Kautz Y, Elgaher W, Pätzold L, Röhrig T, Laschke M, Tschernig T, Hirsch A, Molodtsov V, Murakami K, Hartmann R, Bischoff M (2020)
ACS infectious diseases 6 (10): 2573-2581DOI: 10.1021/acsinfecdis.0c00034
Protein‐Templated Hit Identification through an Ugi Four‐Component Reaction
Federica Mancini, M. Yagiz Unver, Walid A. M. Elgaher, Varsha R. Jumde, Alaa Alhayek, Peer Lukat, Jennifer Herrmann, Martin D. Witte, Matthias Köck, Wulf Blankenfeldt, Rolf Müller, Hirsch A (2020)
Chemistry – A European Journal 26 (64)DOI: 10.1002/chem.202086462
7-Hydroxycoumarins are Affinity-based Fluorescent Probes for Competitive Binding Studies of Macrophage Migration Inhibitory Factor
Xiao Z, Chen D, Song S, van der Vlag R, van der Wouden P, van Merkerk R, Cool R, Hirsch A, Melgert B, Quax W, Poelarends G, Dekker F (2020)
Journal of medicinal chemistryDOI: 10.1021/acs.jmedchem.0c01160
pH-Dependent morphology and optical properties of lysine-derived molecular biodynamers
Lee S, Kaya C, Jang H, Koch M, Loretz B, Buhler E, Lehr C, Hirsch A (2020)
Mater. Chem. Front. 4 (3): 905-909DOI: 10.1039/C9QM00651F
Rapid Discovery of Aspartyl Protease Inhibitors Using an Anchoring Approach
Konstantinidou M, Magari F, Sutanto F, Haupenthal J, Jumde R, Ünver M, Heine A, Camacho C, Hirsch A, Klebe G, Dömling A (2020)
ChemMedChem 15 (8): 680-684DOI: 10.1002/cmdc.202000024
Tracheal brush cells release acetylcholine in response to bitter tastants for paracrine and autocrine signaling
Hollenhorst M, Jurastow I, Nandigama R, Appenzeller S, Li L, Vogel J, Wiederhold S, Althaus M, Empting M, Altmüller J, …, Saliba A, Krasteva-Christ G (2020)
FASEB j. 34 (1): 316-332DOI: 10.1096/fj.201901314RR
Optimized Inhibitors of MDM2 via an Attempted Protein‐Templated Reductive Amination
Vlag R, Yagiz Unver M, Felicetti T, Twarda-Clapa A, Kassim F, Ermis C, Neochoritis C, Musielak B, Labuzek B, Dömling A, Holak T, Hirsch A (2020)
ChemMedChem 15 (4): 370-375DOI: 10.1002/cmdc.201900574
Protein‐Templated Hit Identification via an Ugi Four‐Component Reaction
Mancini F, Unver M, Elgaher W, Jumde V, Alhayek A, Lukat P, Herrmann J, Witte M, Köck M, Blankenfeldt W, Müller R, Hirsch A (2020)
Chem. Eur. J.DOI: 10.1002/chem.202002250
Synthesis and Biological Evaluation of Novel 2-Substituted Analogues of (–)-Pentenomycin I
Zisopoulou S, Bousis S, Haupenthal J, Herrmann J, Müller R, Hirsch A, Komiotis D, Gallos J, Stathakis C (2020)
Synlett 31 (05): 475-481DOI: 10.1055/s-0039-1690772
BOPC1 Enantiomers Preparation and HuR Interaction Study. From Molecular Modeling to a Curious DEEP-STD NMR Application
Della Volpe S, Listro R, Parafioriti M, Di Giacomo M, Rossi D, Ambrosio F, Costa G, Alcaro S, Ortuso F, Hirsch A, Vasile F, Collina S (2020)
ACS medicinal chemistry letters 11 (5): 883-888DOI: 10.1021/acsmedchemlett.9b00659
Validating the 1,2-Difluoro Motif As a Hybrid Bioisostere of CF3 and Et Using Matrix Metalloproteinases As Structural Probes
Erdeljac N, Thiehoff C, Jumde R, Daniliuc C, Höppner S, Faust A, Hirsch A, Gilmour R (2020)
Journal of medicinal chemistry 63 (11): 6225-6237DOI: 10.1021/acs.jmedchem.0c00648
N -Aryl-3-mercaptosuccinimides as Antivirulence Agents Targeting Pseudomonas aeruginosa Elastase and Clostridium Collagenases
Konstantinovic J, Yahiaoui S, Alhayek A, Haupenthal J, Schönauer E, Andreas A, Kany A, Müller R, Koehnke J, Berger F, …, Brandstetter H, Hirsch A (2020)
J. Med. Chem. 63 (15): 8359-8368DOI: 10.1021/acs.jmedchem.0c00584
Flotillin-mediated membrane fluidity controls peptidoglycan synthesis and MreB movement
Zielinska A, Savietto A, Sousa Borges A, Martinez D, Berbon M, Roelofsen J, Hartman A, Boer R, van der Klei I, Hirsch A, …, Bramkamp M, Scheffers D (2020)
eLife 9DOI: 10.7554/eLife.57179
Potential Dental Biofilm Inhibitors: Dynamic Combinatorial Chemistry Affords Sugar-Based Molecules that Target Bacterial Glucosyltransferase
Hartman A, Jumde V, Elgaher W, Te Poele E, Dijkhuizen L, Hirsch A (2020)
ChemMedChemDOI: 10.1002/cmdc.202000222
A rapid synthesis of low-nanomolar divalent LecA inhibitors in four linear steps from d -galactose pentaacetate
Zahorska E, Kuhaudomlarp S, Minervini S, Yousaf S, Lepsik M, Kinsinger T, Hirsch A, Imberty A, Titz A (2020)
Chem. Commun. 56 (62): 8822-8825DOI: 10.1039/d0cc03490h
Novel PqsR Inverse Agonists
Hamed M, Ahmed S, Empting. M., Schütz C, Hartmann R, Röhrig T, Kany A, Hirsch A (2020)
Patent (EP20150119)
2019
Anti-inflammatory and analgesic activity of ointment based on dense ginger extract (Zingiber officinale)
Kravchenko I, Eberle L, Nesterkina M, Kobernik A (2019)
J Herbmed Pharmacol 8 (2): 126-132DOI: 10.15171/jhp.2019.20
Pharmacotherapy of inflammatory process by ginger extract (Zingiber officinale) ointment
Kravchenko I, Eberle L, Nesterkina M, Kobernik A (2019)
J Herbmed Pharmacol 8 (2): 101-107DOI: 10.15171/jhp.2019.16
Analgesic and Anti-Inflammatory Activity of Vanillin Derivatives
Boiko Y, Nesterkina M, Shandra A, Kravchenko I (2019)
Pharm Chem J 53 (7): 650-654DOI: 10.1007/s11094-019-02056-2
Effect of esters based on terpenoids and GABA on fluidity of phospholipid membranes
Nesterkina M, Smola S, Kravchenko I (2019)
J. Liposome Res. 29 (3): 239-246DOI: 10.1080/08982104.2018.1538238
(2S,5R)-2-Isopropyl-5-methylcyclohexanone Hydrazones
Nesterkina M, Barbalat D, Zheltvay I, Rakipov I, Atakay M, Salih B, Kravchenko I (2019)
Molbank 2019 (2)DOI: 10.3390/M1062
Energy-Coupling Factor Transporters as Novel Antimicrobial Targets
Bousis S, Setyawati I, Diamanti E, Slotboom D, Hirsch A (2019)
Advanced Therapeutics, 2, 1800066DOI: 10.1002/ADTP.201800066
Protein-Templated Dynamic Combinatorial Chemistry: Brief Overview and Experimental Protocol
Hartman A, Gierse R, Hirsch A (2019)
European journal of organic chemistry 2019 (22): 3581-3590DOI: 10.1002/ejoc.201900327
Concepts and Core Principles of Fragment-Based Drug Design
Kirsch P, Hartman A, Hirsch A, Empting M (2019)
Molecules (Basel, Switzerland) 24 (23)DOI: 10.3390/molecules24234309
Comparing the Self-Assembly of Sexiphenyl-Dicarbonitrile on Graphite and Graphene on Cu(111)
Schmidt N, Li J, Gottardi S, Moreno-Lopez J, Enache M, Monjas L, van der Vlag R, Havenith R, Hirsch A, Stöhr M (2019)
Chem. Eur. J. 25 (19): 5065-5070DOI: 10.1002/chem.201806312
Inverting Small Molecule–Protein Recognition by the Fluorine Gauche Effect: Selectivity Regulated by Multiple H→F Bioisosterism
Bentler P, Bergander K, Daniliuc C, Mück-Lichtenfeld C, Jumde R, Hirsch A, Gilmour R (2019)
Angewandte Chemie (International ed. in English) 58 (32): 10990-10994DOI: 10.1002/anie.201905452
Spray-drying of inhalable, multifunctional formulations for the treatment of biofilms formed in cystic fibrosis
Lababidi N, Ofosu Kissi E, Elgaher W, Sigal V, Haupenthal J, Schwarz B, Hirsch A, Rades T, Schneider M (2019)
Journal of Controlled Release 314: 62-71DOI: 10.1016/j.jconrel.2019.10.038
From Wood to Tetrahydro-2-benzazepines in Three Waste-Free Steps: Modular Synthesis of Biologically Active Lignin-Derived Scaffolds
Elangovan S, Afanasenko A, Haupenthal J, Sun Z, Liu Y, Hirsch A, Barta K (2019)
ACS Cent. Sci. 5 (10): 1707-1716DOI: 10.1021/acscentsci.9b00781
Surface state tunable energy and mass renormalization from homothetic quantum dot arrays
Piquero-Zulaica I, Li J, Abd El-Fattah Z, Solianyk L, Gallardo I, Monjas L, Hirsch A, Arnau A, Ortega J, Stöhr M, Lobo-Checa J (2019)
Nanoscale 11 (48): 23132-23138DOI: 10.1039/c9nr07365e
Novel Compounds Targeting the RNA-Binding Protein HuR. Structure-Based Design, Synthesis, and Interaction Studies
Della Volpe S, Nasti R, Queirolo M, Unver M, Jumde V, Dömling A, Vasile F, Potenza D, Ambrosio F, Costa G, …, Hirsch A, Collina S (2019)
ACS Med. Chem. Lett. 10 (4): 615-620DOI: 10.1021/acsmedchemlett.8b00600
A combinatorial approach for the discovery of drug-like inhibitors of 15-lipoxygenase-1
van der Vlag R, Guo H, Hapko U, Eleftheriadis N, Monjas L, Dekker F, Hirsch A (2019)
European journal of medicinal chemistry 174: 45-55DOI: 10.1016/j.ejmech.2019.04.021
Rational Adaptation of L3MBTL1 Inhibitors to Create Small-Molecule Cbx7 Antagonists
Simhadri C, Daze K, Douglas S, Milosevich N, Monjas L, Dev A, Brown T, Hirsch A, Wulff J, Hof F (2019)
ChemMedChem 14 (15): 1444-1456DOI: 10.1002/cmdc.201900021
Low-Dimensional Metal-Organic Coordination Structures on Graphene
Li J, Solianyk L, Schmidt N, Baker B, Gottardi S, Moreno Lopez J, Enache M, Monjas L, van der Vlag R, Havenith R, Hirsch A, Stöhr M (2019)
The journal of physical chemistry. C, Nanomaterials and interfaces 123 (20): 12730-12735DOI: 10.1021/acs.jpcc.9b00326
Novel 15-Lipoxygenase-1 Inhibitor Protects Macrophages from Lipopolysaccharide-Induced Cytotoxicity
Guo H, Verhoek I, Prins G, van der Vlag R, van der Wouden P, van Merkerk R, Quax W, Olinga P, Hirsch A, Dekker F (2019)
Journal of medicinal chemistry 62 (9): 4624-4637DOI: 10.1021/acs.jmedchem.9b00212
Replacement of an Indole Scaffold Targeting Human 15-Lipoxygenase-1 Using Combinatorial Chemistry
Prismawan D, van der Vlag R, Guo H, Dekker F, Hirsch A (2019)
HCA 102 (5)DOI: 10.1002/hlca.201900040
Reversible immobilization of a protein to a gold surface through multiple host-guest interactions
Schwarz D, Elgaher W, Hollemeyer K, Hirsch A, Wenz G (2019)
J. Mater. Chem. B 7 (40): 6148-6155DOI: 10.1039/c9tb00560a
2018
Repellent activity of monoterpenoid esters with neurotransmitter amino acids against yellow fever mosquito, Aedes aegypti
Nesterkina M, Bernier U, Tabanca N, Kravchenko I (2018)
Open Chemistry 16 (1): 95-98DOI: 10.1515/chem-2018-0015
The influence of monoterpenoids and phenol derivatives on Drosophila melanogaster viability
Nesterkina M, Bilokon S, Alieksieieva T, Chubyk I, Kravchenko I (2018)
Journal of Asia-Pacific Entomology 21 (3): 793-796DOI: 10.1016/j.aspen.2018.06.004
Trendbericht Biochemie 2017: Proteinvermittelte dynamische kombinatorische Chemie
Hirsch A (2018)
Nachr. Chem. 66 (3): 281-283DOI: 10.1002/nadc.20184071734
Druggability Assessment of Targets Used in Kinetic Target-Guided Synthesis
Unver M, Gierse R, Ritchie H, Hirsch A (2018)
Journal of medicinal chemistry 61 (21): 9395-9409DOI: 10.1021/acs.jmedchem.8b00266
Phage Display on the Anti-infective Target 1-Deoxy-d-xylulose-5-phosphate Synthase Leads to an Acceptor-Substrate Competitive Peptidic Inhibitor
Marcozzi A, Masini T, Di Zhu, Pesce D, Illarionov B, Fischer M, Herrmann A, Hirsch A (2018)
ChemBioChem 19 (1): 58-65DOI: 10.1002/cbic.201700402
Lipid-DNAs as Solubilizers of m THPC
Liu Y, de Vries J, Liu Q, Hartman A, Wieland G, Wieczorek S, Börner H, Wiehe A, Buhler E, Stuart M, …, Herrmann A, Hirsch A (2018)
Chem. Eur. J. 24 (4): 798-802DOI: 10.1002/chem.201705206
Glucansucrase (mutant) enzymes from Lactobacillus reuteri 180 efficiently transglucosylate Stevia component rebaudioside A, resulting in a superior taste
Te Poele E, Devlamynck T, Jäger M, Gerwig G, van de Walle D, Dewettinck K, Hirsch A, Kamerling J, Soetaert W, Dijkhuizen L (2018)
Sci. Rep. 8 (1)DOI: 10.1038/s41598-018-19622-5
Delivery system for budesonide based on lipid-DNA
Liu Y, Bos I, Oenema T, Meurs H, Maarsingh H, Hirsch A (2018)
European journal of pharmaceutics and biopharmaceutics : official journal of Arbeitsgemeinschaft fur Pharmazeutische Verfahrenstechnik e.V 130: 123-127DOI: 10.1016/j.ejpb.2018.06.012
Dynamic Proteoids Generated From Dipeptide-Based Monomers
Liu Y, Stuart M, Buhler E, Hirsch A (2018)
Macromolecular rapid communications 39 (13)DOI: 10.1002/marc.201800099
Design and Synthesis of Bioisosteres of Acylhydrazones as Stable Inhibitors of the Aspartic Protease Endothiapepsin
Jumde V, Mondal M, Gierse R, Unver M, Magari F, van Lier R, Heine A, Klebe G, Hirsch A (2018)
ChemMedChem 13 (21): 2266-2270DOI: 10.1002/cmdc.201800446
Exploration of ligand binding modes towards the identification of compounds targeting HuR: a combined STD-NMR and Molecular Modelling approach
Vasile F, Della Volpe S, Ambrosio F, Costa G, Unver M, Zucal C, Rossi D, Martino E, Provenzani A, Hirsch A, …, Potenza D, Collina S (2018)
Sci. Rep. 8 (1)DOI: 10.1038/s41598-018-32084-z
Donepezil-melatonin hybrids as butyrylcholinesterase inhibitors: Improving binding affinity through varying mode of linking fragments
Lozinska I, Swierczynska A, Moleda Z, Hartman A, Hirsch A, Czarnocki Z (2018)
Archiv der Pharmazie 351 (11)DOI: 10.1002/ardp.201800194
2017
Synthesis and Pharmacological Properties of Novel Esters Based on Monoterpenoids and Glycine
Nesterkina M, Kravchenko I (2017)
Pharmaceuticals (Basel, Switzerland) 10 (2)DOI: 10.3390/ph10020047
(1R,2S,5R)-2-Isopropyl-5-methylcyclohexyl 4-Aminobutyrate Hydrochloride
Nesterkina M, Shishkina S, Maltsev G, Rakipov I, Kravchenko I (2017)
Molbank 2017 (3)DOI: 10.3390/M956
Molecular Biodynamers: Dynamic Covalent Analogues of Biopolymers
Liu Y, Lehn J, Hirsch A (2017)
Accounts of chemical research 50 (2): 376-386DOI: 10.1021/acs.accounts.6b00594
DXS as a target for structure-based drug design
Gierse R, Redeem E, Diamanti E, Wrenger C, Groves M, Hirsch A (2017)
Future medicinal chemistry 9 (11): 1277-1294DOI: 10.4155/fmc-2016-0239
Molecular insight into specific 14-3-3 modulators: Inhibitors and stabilisers of protein-protein interactions of 14-3-3
Hartman A, Hirsch A (2017)
European journal of medicinal chemistry 136DOI: 10.1016/j.ejmech.2017.04.058
Compounds Interfering with Embryonic Lethal Abnormal Vision (ELAV) Protein-RNA Complexes: An Avenue for Discovering New Drugs
Nasti R, Rossi D, Amadio M, Pascale A, Unver M, Hirsch A, Collina S (2017)
Journal of medicinal chemistry 60 (20): 8257-8267DOI: 10.1021/acs.jmedchem.6b01871
Fine-tuning Nanocarriers Specifically toward Cargo: A Competitive Study on Solubilizing Related Photosensitizers for Photodynamic Therapy
Wieczorek S, Remmler D, Masini T, Kochovski Z, Hirsch A, Börner H (2017)
Bioconjugate chemistry 28 (3): 760-767DOI: 10.1021/acs.bioconjchem.6b00549
Pentapeptide‐rich peptidoglycan at the Bacillus subtilis cell‐division site
Morales Angeles D, Liu Y, Hartman A, Borisova M, Sousa Borges A, Kok N, Beilharz K, veening j, Mayer C, Hirsch A, Scheffers D (2017)
Molecular microbiology 104 (2): 319-333DOI: 10.1111/mmi.13629
Bicyclic enol cyclocarbamates inhibit penicillin-binding proteins
Dockerty P, Edens J, Tol M, Morales Angeles D, Domenech A, Liu Y, Hirsch A, veening j, Scheffers D, Witte M (2017)
Organic & biomolecular chemistry 15 (4): 894-910DOI: 10.1039/c6ob01664b
Designed Spiroketal Protein Modulation
Scheepstra M, Andrei S, Unver M, Hirsch A, Leysen S, Ottmann C, Brunsveld L, Milroy L (2017)
Angewandte Chemie (International ed. in English) 56 (20): 5480-5484DOI: 10.1002/anie.201612504
Insight into the complete substrate-binding pocket of ThiT by chemical and genetic mutations
Swier L, Monjas L, Reeßing F, Oudshoorn R, Aisyah, Primke T, Bakker M, van Olst E, Ritschel T, Faustino I, …, Hirsch A, Slotboom D (2017)
MedChemComm 8 (5): 1121-1130DOI: 10.1039/c7md00079k
Saccharide-Containing Dynamic Proteoids
Liu Y, Stuart M, Witte M, Buhler E, Hirsch A (2017)
Chemistry (Weinheim an der Bergstrasse, Germany) 23 (64): 16162-16166DOI: 10.1002/chem.201703584
Dynamic Combinatorial Chemistry to Identify Binders of ThiT, an S-Component of the Energy-Coupling Factor Transporter for Thiamine
Monjas L, Swier L, Setyawati I, slotboom d, Hirsch A (2017)
ChemMedChem 12 (20): 1693-1696DOI: 10.1002/cmdc.201700440
In-depth Profiling of MvfR-Regulated Small Molecules in Pseudomonas aeruginosa after Quorum Sensing Inhibitor Treatment
Allegretta G, Maurer C, Eberhard J, Maura D, Hartmann R, Rahme L, Empting M (2017)
Frontiers in microbiology 8DOI: 10.3389/fmicb.2017.00924
2016
Synthesis and Anticonvulsant Activity of Menthyl γ-Aminobutyrate
Nesterkina M, Kravchenko I (2016)
Chem Nat Compd 52 (2): 237-239DOI: 10.1007/s10600-016-1604-9
Synthesis and Anticonvulsant Activity of New Calix[4]Arene Derivatives Containing Gamma-Aminobutyric Acid Moieties
Nesterkina M, Alekseeva E, Kravchenko I (2016)
Pharm Chem J 49 (12): 825-829DOI: 10.1007/s11094-016-1380-7
Synthesis and Pharmacological Properties of Novel Esters Based on Monocyclic Terpenes and GABA
Nesterkina M, Kravchenko I (2016)
Pharmaceuticals (Basel, Switzerland) 9 (2)DOI: 10.3390/ph9020032
Analgesic Activity of Novel GABA Esters after Transdermal Delivery
Nesterkina M, Kravchenko I (2016)
Nat. Prod. Commun. 11 (10)DOI: 10.1177/1934578X1601101001
Design and synthesis of thiamine analogues to study their binding to the ECF transporter for thiamine in bacteria
Monjas L, Swier L, Voogd A, Oudshoorn R, Hirsch A, Slotboom D (2016)
Med. Chem. Commun. 7 (5): 966-971DOI: 10.1039/C6MD00022C
Furoates and thenoates inhibit pyruvate dehydrogenase kinase 2 allosterically by binding to its pyruvate regulatory site
Masini T, Birkaya B, van Dijk S, Mondal M, Hekelaar J, Jäger M, van Terwisscha Scheltinga A, Patel M, Hirsch A, Moman E (2016)
Journal of enzyme inhibition and medicinal chemistry 31 (sup4): 170-175DOI: 10.1080/14756366.2016.1201812
Proteoid Dynamers with Tunable Properties
Liu Y, Stuart M, Buhler E, Lehn J, Hirsch A (2016)
Fragment Linking and Optimization of Inhibitors of the Aspartic Protease Endothiapepsin: Fragment-Based Drug Design Facilitated by Dynamic Combinatorial Chemistry
Mondal M, Radeva N, Fanlo-Virgós H, Otto S, Klebe G, Hirsch A (2016)
Angewandte Chemie (International ed. in English) 55 (32): 9422-6DOI: 10.1002/anie.201603074
Fragment-Based Drug Design Facilitated by Protein-Templated Click Chemistry: Fragment Linking and Optimization of Inhibitors of the Aspartic Protease Endothiapepsin
Mondal M, Unver M, Pal A, Bakker M, Berrier S, Hirsch A (2016)
Chem. Eur. J. 22 (42): 14826-14830DOI: 10.1002/chem.201603001
Application of Dual Inhibition Concept within Looped Autoregulatory Systems toward Antivirulence Agents against Pseudomonas aeruginosa Infections
Thomann A, Mello Martins A, Brengel C, Empting M, Hartmann R (2016)
ACS chemical biology 11 (5): 1279-86DOI: 10.1021/acschembio.6b00117
Novel Strategies for the Treatment of Pseudomonas aeruginosa Infections
Wagner S, Sommer R, Hinsberger S, Lu C, Hartmann R, Empting M, Titz A (2016)
Journal of medicinal chemistry 59 (13): 5929-69DOI: 10.1021/acs.jmedchem.5b01698
Discovery of the first small-molecule CsrA-RNA interaction inhibitors using biophysical screening technologies
Maurer C, Fruth M, Empting M, Avrutina O, Hossmann J, Nadmid S, Gorges J, Herrmann J, Kazmaier U, Dersch P, Muller R, Hartmann R (2016)
Future medicinal chemistry 8 (9): 931-47DOI: 10.4155/fmc-2016-0033
Discovery and Structure-Based Optimization of 2-Ureidothiophene-3-carboxylic Acids as Dual Bacterial RNA Polymerase and Viral Reverse Transcriptase Inhibitors
Elgaher W, Sharma K, Haupenthal J, Saladini F, Pires M, Real E, Mely Y, Hartmann R (2016)
Journal of medicinal chemistryDOI: 10.1021/acs.jmedchem.6b00730
Dissecting the Multiple Roles of PqsE in Pseudomonas aeruginosa Virulence by Discovery of Small Tool Compounds
Zender M, Witzgall F, Drees S, Weidel E, Maurer C, Fetzner S, Blankenfeldt W, Empting M, Hartmann R (2016)
ACS chemical biologyDOI: 10.1021/acschembio.6b00156
2015
Dynamic combinatorial chemistry: a tool to facilitate the identification of inhibitors for protein targets
Mondal M, Hirsch A (2015)
Chemical Society reviews 44 (8): 2455-88DOI: 10.1039/c4cs00493k
Fighting malaria: structure-guided discovery of nonpeptidomimetic plasmepsin inhibitors
Huizing A, Mondal M, Hirsch A (2015)
Journal of medicinal chemistry 58 (13): 5151-63DOI: 10.1021/jm5014133
Harnessing dynamic combinatorial chemistry in the search for new ligands for protein targets
Monjas L, Hirsch A (2015)
Future medicinal chemistry 7 (16): 2095-8DOI: 10.4155/fmc.15.146
Combinatorial screening for specific drug solubilizers with switchable release profiles
Wieczorek S, Vigne S, Masini T, Ponader D, Hartmann L, Hirsch A, Börner H (2015)
Macromolecular Bioscience 15 (1): 82-9DOI: 10.1002/mabi.201400443
Structure-based design of potent small-molecule binders to the S-component of the ECF transporter for thiamine
Swier L, Monjas L, Guskov A, Voogd A, Erkens G, slotboom d, Hirsch A (2015)
ChemBioChem 16 (5): 819-26DOI: 10.1002/cbic.201402673
Fragment growing exploiting dynamic combinatorial chemistry of inhibitors of the aspartic protease endothiapepsin
Mondal M, Groothuis D, Hirsch A (2015)
DOI: 10.1039/C5MD00157A
Structure-Based Optimization of Inhibitors of the Aspartic Protease Endothiapepsin
Hartman A, Mondal M, Radeva N, Klebe G, Hirsch A (2015)
International journal of molecular sciences 16 (8): 19184-94DOI: 10.3390/ijms160819184
Supramolecular chemistry … and beyond
Hirsch A (2015)
Angewandte Chemie (International ed. in English) 54 (38): 11013-4DOI: 10.1002/anie.201506536
Validation of a homology model of Mycobacterium tuberculosis DXS: rationalization of observed activities of thiamine derivatives as potent inhibitors of two orthologues of DXS
Masini T, Lacy B, Monjas L, Hawksley D, Voogd A, Illarionov B, Iqbal A, Leeper F, Fischer M, Kontoyianni M, Hirsch A (2015)
Organic & biomolecular chemistry 13 (46): 11263-77DOI: 10.1039/c5ob01666e
Exploring the chemical space of ureidothiophene-2-carboxylic acids as inhibitors of the quorum sensing enzyme PqsD from Pseudomonas aeruginosa
Sahner J, Empting M, Kamal A, Weidel E, Groh M, Börger C, Hartmann R (2015)
European journal of medicinal chemistry 96: 14-21DOI: 10.1016/j.ejmech.2015.04.007
Novel PqsR Inverse Agonists
Hamed M (2015)
Patent (EP 201523196)
Advanced mutasynthesis studies on the natural α-pyrone antibiotic myxopyronin from Myxococcus fulvus
Sahner J, Sucipto H, Wenzel S, Groh M, Hartmann R, Müller R (2015)
ChemBioChem 16: 946-953DOI: 10.1002/cbic.201402666
2014
Synthesis, Physicochemical Properties, and Anticonvulsant Activity of the Gaba Complex with a Calix[4]Arene derivative
Nesterkina M, Alekseeva E, Kravchenko I (2014)
Pharm Chem J 48 (2): 82-84DOI: 10.1007/s11094-014-1052-4
Development of inhibitors of the 2C-methyl-D-erythritol 4-phosphate (MEP) pathway enzymes as potential anti-infective agents
Masini T, Hirsch A (2014)
Journal of medicinal chemistry 57 (23): 9740-63DOI: 10.1021/jm5010978
Theoretical and structural analysis of long C-C bonds in the adducts of polycyanoethylene and anthracene derivatives and their connection to the reversibility of Diels-Alder reactions
Hirsch A, Reutenauer P, Le Moignan M, Ulrich S, Boul P, Harrowfield J, Jarowski P, Lehn J (2014)
Chemistry (Weinheim an der Bergstrasse, Germany) 20 (4): 1073-80DOI: 10.1002/chem.201303276
Structure-based design of inhibitors of the aspartic protease endothiapepsin by exploiting dynamic combinatorial chemistry
Mondal M, Radeva N, Köster H, Park A, Potamitis C, Zervou M, Klebe G, Hirsch A (2014)
Angewandte Chemie (International ed. in English) 53 (12): 3259-63DOI: 10.1002/anie.201309682
A natural-product switch for a dynamic protein interface
Scheepstra M, Nieto L, Hirsch A, Fuchs S, Leysen S, Lam C, het Panhuis L, van Boeckel C, Wienk H, Boelens R, …, Milroy L, Brunsveld L (2014)
Angewandte Chemie (International ed. in English) 53 (25): 6443-8DOI: 10.1002/anie.201403773
A doubly hermaphroditic chiral crown ether
Hirsch A, Sirlin C, Harrowfield J, Lehn J (2014)
DOI: 10.1039/C4CE00879K
De novo fragment-based design of inhibitors of DXS guided by spin-diffusion-based NMR spectroscopy
Masini T, Pilger J, Kroezen B, Illarionov B, Lottmann P, Fischer M, Griesinger C, Hirsch A (2014)
Chem. Sci. 5 (9): 3543-3551DOI: 10.1039/C4SC00588K
From in vitro to in cellulo: structure-activity relationship of (2-nitrophenyl)methanol derivatives as inhibitors of PqsD in Pseudomonas aeruginosa
Storz M, Allegretta G, Kirsch B, Empting M, Hartmann R (2014)
Organic & biomolecular chemistry 12 (32): 6094-104DOI: 10.1039/c4ob00707g
Benzamidobenzoic acids as potent PqsD inhibitors for the treatment of Pseudomonas aeruginosa infections
Hinsberger S, Jong J, Groh M, Haupenthal J, Hartmann R (2014)
European journal of medicinal chemistry 76: 343-51DOI: 10.1016/j.ejmech.2014.02.014
Overcoming the unexpected functional inversion of a PqsR antagonist in Pseudomonas aeruginosa: an in vivo potent antivirulence agent targeting pqs quorum sensing
Lu C, Maurer C, Kirsch B, Steinbach A, Hartmann R (2014)
Angewandte Chemie (International ed. in English) 53 (4): 1109-12DOI: 10.1002/anie.201307547
2013
Druggability of the enzymes of the non-mevalonate-pathway
Masini T, Kroezen B, Hirsch A (2013)
Drug Discovery Today 18 (23-24): 1256-62DOI: 10.1016/j.drudis.2013.07.003
Total synthesis, stereochemical elucidation and biological evaluation of Ac 2 SGL; a 1,3-methyl branched sulfoglycolipid from Mycobacterium tuberculosis
Geerdink D, Horst B, Lepore M, Mori L, Puzo G, Hirsch A, Gilleron M, Libero G, Minnaard A (2013)
DOI: 10.1039/C2SC21620E
Imidazole- and Benzimidazole-Based Inhibitors of the Kinase IspE: Targeting the Substrate-Binding Site and the Triphosphate-Binding Loop of the ATP Site
Mombelli P, Le Chapelain C, Munzinger N, Joliat E, Illarionov B, Schweizer W, Hirsch A, Fischer M, Bacher A, Diederich F (2013)
Exploiting specific interactions toward next-generation polymeric drug transporters
Wieczorek S, Krause E, Hackbarth S, Röder B, Hirsch A, Börner H (2013)
Journal of the American Chemical Society 135 (5): 1711-4DOI: 10.1021/ja311895z
2012
Total synthesis of (-)-doliculide, structure-activity relationship studies and its binding to F-actin
Matcha K, Madduri A, Roy S, Ziegler S, Waldmann H, Hirsch A, Minnaard A (2012)
ChemBioChem 13 (17): 2537-48DOI: 10.1002/cbic.201200512
The isoprenoid-precursor dependence of Plasmodium spp
van der Meer J, Hirsch A (2012)
Natural product reports 29 (7): 721-8DOI: 10.1039/c2np20013a
Metal-ion-induced shape switching: Stereoselective formation of a dinuclear Hg(II) double helicate from a hydrazonobis(acylhydrazone) ligand
Schaeffer G, Harrowfield J, Lehn J, Hirsch A (2012)
Biodynamers: self-organization-driven formation of doubly dynamic proteoids
Hirsch A, Buhler E, Lehn J (2012)
Journal of the American Chemical Society 134 (9): 4177-83DOI: 10.1021/ja2099134
Exploring the Ribose Sub-Pocket of the Substrate-Binding Site in Escherichia coli IspE: Structure-Based Design, Synthesis, and Biological Evaluation of Cytosines and Cytosine Analogues
Schütz A, Osawa S, Mathis J, Hirsch A, Bernet B, Illarionov B, Fischer M, Bacher A, Diederich F (2012)
2009
SYNTHESIS, ANTI-BRONCHOCONSTRICTIVE, AND ANTIBACTERIAL ACTIVITIES OF SOME NEW 8- SUBSTITUTED-1,3-DIMETHYLXANTHINE DERIVATIVES
Elgaher W, Hayallah A, Salem O, Abdel Alim A (2009)
Bulletin of Pharmaceutical Sciences. Assiut 32 (1): 153-187DOI: 10.21608/BFSA.2009.63355
Bioconjugates to specifically render inhibitors water-soluble
Hirsch A, Diederich F, Antonietti M, Börner H (2009)
Soft Matter 6 (1): 88-91DOI: 10.1039/B915928B
2008
The Non-Mevalonate Pathway to Isoprenoid Biosynthesis: A Potential Source of New Drug Targets
Hirsch A, Diederich F (2008)
CHIMIA 62 (4): 226-230DOI: 10.2533/chimia.2008.226
Synthesis and characterization of cytidine derivatives that inhibit the kinase IspE of the non-mevalonate pathway for isoprenoid biosynthesis
Crane C, Hirsch A, Alphey M, Sgraja T, Lauw S, Illarionova V, Rohdich F, Eisenreich W, Hunter W, Bacher A, Diederich F (2008)
ChemMedChem 3 (1): 91-101DOI: 10.1002/cmdc.200700208
Inhibitors of the kinase IspE: structure-activity relationships and co-crystal structure analysis
Hirsch A, Alphey M, Lauw S, Seet M, Barandun L, Eisenreich W, Rohdich F, Hunter W, Bacher A, Diederich F (2008)
Organic & biomolecular chemistry 6 (15): 2719-30DOI: 10.1039/b804375b
2007
Phosphate recognition in structural biology
Hirsch A, Fischer F, Diederich F (2007)
Angewandte Chemie (International ed. in English) 46 (3): 338-52DOI: 10.1002/anie.200603420
Nonphosphate inhibitors of IspE protein, a kinase in the non-mevalonate pathway for isoprenoid biosynthesis and a potential target for antimalarial therapy
Hirsch A, Lauw S, Gersbach P, Schweizer W, Rohdich F, Eisenreich W, Bacher A, Diederich F (2007)
ChemMedChem 2 (6): 806-10DOI: 10.1002/cmdc.200700014
2006
Double conjugate addition of dithiols to propargylic carbonyl systems to generate protected 1,3-dicarbonyl compounds
Sneddon H, van den Heuvel A, Hirsch A, Booth R, Shaw D, Gaunt M, Ley S (2006)
The Journal of organic chemistry 71 (7): 2715-25DOI: 10.1021/jo052514s