NMR-Spektroskopie
NMR-Spektroskopie ist eine der wichtigsten Methoden im Bereich der Strukturaufklärung und –verifizierung. Unsere NMR-Geräte werden sowohl routinemäßig für 1D- und 2D-Standardmessungen, z.B. zur Reaktionskontrolle in der organischen Synthese genutzt, als auch für de novo Strukturaufklärungen und fortgeschrittene Messmethoden. Unsere NMR-Abteilung umfasst drei unterschiedliche Geräte, von denen jedes einen eigenen Anwendungsschwerpunkt hat:
Avance III Spektrometer, UltraShield 500 MHz, He-gekühlte 5 mm TCI CryoProbe (‘inverse’)
Avance III Spektrometer, Ascend 700 MHz, He- gekühlte 5 mm TCI CryoProbe (‘inverse’)
Avance Neo Spektrometer, UltraShield Plus 500 MHz, N2- gekühlte 5 mm Prodigy BBO-CryoProbe (‘observe’) mit Autosampler.
Zebrafischlabor
Zebrafische (Danio rerio) gehören zu den wichtigsten Wirbeltier-Modellorganismen von Nicht-Säugetieren. Besonders die Larven sind von Interesse, da die Embryonalentwicklung sehr schnell ist und die Larven relativ groß, robust und transparent sind.
Seit 2017 ist die Zebrafischanlage am HIPS voll funktionsfähig. Sie hat ein Systemvolumen von 3.500 Litern und eine Gesamtkapazität von mehr als 25.000 Tieren. Zurzeit stehen zwei Wildtyp-Stämme sowie mehrere Mutanten- bzw. transgene Modelle zur Verfügung. In unserem S2-Labor stehen zwei Mikroinjektionsstationen zur Verfügung, die aus Fluoreszenz-Stereomikroskopen mit Druckinjektoren und Mikromanipulatoren bestehen.
Am HIPS verwenden wir Zebrafischlarven hauptsächlich um Naturstoffe auf ihre potenzielle Toxizität und ihre maximal tolerierte Konzentration (MTC) zu untersuchen. Des Weiteren verfügen wir über mehrere Infektionsmodelle zur frühen in vivo Profilierung. Im Zuge von DMPK-Studien (drug metabolism and pharmacokinetics) wurde zudem ein neues bildgebendes Verfahren etabliert, um die räumliche Verteilung von chemischen Verbindungen und deren Stoffwechselprodukten in Zebrafischlarven mittels Massenspektrometrie-Imaging (MSI) zu untersuchen.
Proteinkristallographie
Das Bestimmen hochaufgelöster Proteinstrukturen mittels Röntgenkristallographie ist ein mehrstufiger Prozess. Zunächst muss das zu untersuchende Protein in löslicher und gefalteter Form exprimiert werden. Hierzu verwenden wir sowohl bakterielle als auch auf Säugerzellen basierende Expressionssysteme, welche eine schnelle und einfache Überprüfung vieler Expressionsbedingungen ermöglichen. Sobald die passenden Bedingungen gefunden wurden, ist eine Expression und Aufreinigung im Maßstab von wenigen µg bis hin zu >100 mg möglich. Robotergestützte Systeme ermöglichen die parallele Prüfung einer Vielzahl an Kristallisierungsbedingungen und benötigen nur eine sehr geringe Menge an Ausgangsmaterial (150 nL pro Bedingung). Diese Bedingungen werden anschließend optimiert um Kristalle in der für die Strukturaufklärung notwendigen Qualität zu erhalten. Die Datenerfassung an Synchrotrons ermöglicht die Bestimmung der Struktur des Zielproteins mit atomarer Auflösung, falls notwendig auch im Komplex mit anderen Proteinen oder kleinen Molekülen.
Biophysikalische Methoden
Am Helmholtz-Institut werden neue Antiinfektiva in einem iterativen Prozess entwickelt, der zahlreiche Optimierungsschritte umfasst. In diesem Zusammenhang ist es unerlässlich, biomolekulare Interaktionen wie die Bindung eines Wirkstoffs (Liganden) an seine Zielstruktur, meist ein definiertes Protein, zu untersuchen. Eine genaue qualitative und quantitative Aussage über eine solche biomolekulare Interaktion ist Voraussetzung für den weiteren Optimierungsprozess.
Auf der biophysikalischen Testplattform des HIPS werden unterschiedliche Technologien zur Untersuchung solcher biomolekularen Wechselwirkungen eingesetzt. Diese umfassen die Oberflächen-Plasmonenresonanz (SPR), die Differential Scanning Fluorimetrie (DSF), die MicroScale Thermophorese (MST) und die Isotherme Titrationskalorimetrie (ITC). In Abhängigkeit der molekularen Eigenschaften und Verfügbarkeiten der Interaktions-Partner wird entschieden, welche der biophysikalischen Methoden zum Einsatz kommt.
Mikroskopie
Durch die Kombination hochmoderner Technologien wie Fluoreszenz- und Raster-Elektronen Mikroskopie, ist am HIPS sowohl funktionale aus auch molekulare Bildgebung möglich. Hierzu zählt die Visualisierung und Charakterisierung von mikro- und nanoskaligen Arzneistofftransportsystemen und physiologischen, biochemischen und infektiösen Phänomenen in in vivo/in vitro Systemen.
Neben einem Fluoreszenz-Mikroskop (Nikon Eclipse Ti-S), welches zur Untersuchung von biologischen, wie auch anorganischen Proben dient, steht ein Konfokal-Mikroskop (Leica DMi8 inverted microcope) zur Verfügung. Dies ist in der Lage detaillierte Strukturen in verschiedenen optischen Schichten aufzulösen. Damit ist eine hochauflösende 3D Rekonstruktion von Proben möglich. Durch Fluoreszenzmarkierung von Proben ist eine Visualisierung von zellulären Kompartimente, zelluläre Wachstumsmuster, Biofilm-Strukturen oder -Verteilung, die Internalisierung und subzelluläre Lokalisation von Arzneistoffen und Arzneistofftransportsystemen innerhalb der Zellen oder des Gewebes möglich.
Das Raster-Elektronen-Mikroskop (SEM EVA HD15) ist in der Lage hochauflösende Bilder zu generieren. Hierdurch kann man Informationen über die Proben Oberfläche (zum Beispiel Forum und Größe von Partikel) und ihre Zusammensetzung (zum Beispiel Partikelgrößenverteilung innerhalb der Probe) erhalten.
ADMET-Plattform
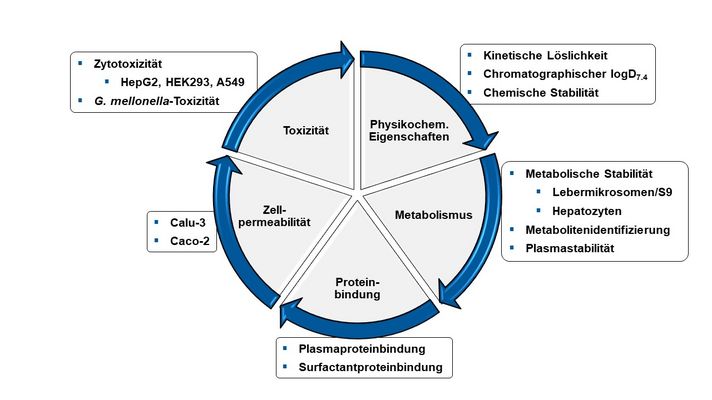
In der translationalen Phase der akademischen Wirkstoffforschung geht es darum, Projekte von der Laborbank in die klinische Anwendung zu bringen („from bench to bedside“). Hierbei fokussieren wir uns verstärkt auf die Bestimmung von in vitro ADMET-Eigenschaften (Absorption, Distribution, Metabolismus, Exkretion und Toxizität). Für erfolgreiche Wirkstoffforschung ist es von enormer Wichtigkeit, diese pharmakokinetischen Eigenschaften potentieller neuer Wirkstoffkandidaten in einem Projekt frühzeitig zu betrachten. Zu diesem Zweck haben wir am HIPS eine rationale in vitro-Screening-Kaskade etabliert, um ADMET-Eigenschaften zu analysieren, wie z.B. kinetische Löslichkeit/logD7.4, metabolische Stabilität/Plasmastabilität in diversen Spezies, Zellpermeabilität, Plasmaproteinbindung und Zytotoxizität. Die Technologien, die wir hierzu verwenden, umfassen UHPLC-MS/MS (TripleQuad/Orbitrap), was zudem auch Studien zur Metabolitenidentifizierung ermöglicht.
Kontinuierliches Screening von ADMET-Eigenschaften begleitet die Optimierung von Verbindungen in unseren internen Projekten sowie in Zusammenarbeit mit externen Gruppen. Die hierbei erzeugten Resultate dienen als Grundlage für die Auswahl von Verbindungen für in vivo-Experimente, wie beispielsweise in unserem Zebrafischlabor.