![[Translate to Deutsch:] [Translate to Deutsch:]](/fileadmin/HIPS/__processed__/c/5/csm_HIPS_50503_431fe075f3.jpg)
Dr. Walid A. M. Elgaher
Wir nutzen verschiedene medizinchemische Ansätze zur effizienten Wirkstoffentdeckung und zielen auf bisher unerschlossene Wirkstofftargets ab. Molekulare Wechselwirkungen zwischen niedermolekularen Liganden und ihren Partnermakromolekülen werden durch eine Kombination biophysikalischer und computergestützter Methoden charakterisiert, um Affinität, Selektivität und Sicherheit zu optimieren.
Unsere Forschung
Unsere Forschung dreht sich um die Entdeckung und Charakterisierung von niedermolekularen Therapeutika mit beispiellosem Wirkmechanismus (MoA) für dringende Gesundheitsprobleme wie antimikrobielle Resistenz, Krebs und neurodegenerative Erkrankungen. Zur Identifizierung bioaktiver Verbindungen wenden wir mehrere Strategien an, darunter Struktur- und Liganden-basiertes Arzneimitteldesign, virtuelles Screening, Fragment-basierte Arzneimittelentdeckung und zielgerichtete Liganden-Assemblierung. Synthese, Reinigung und Strukturaufklärung der entwickelten Moleküle werden mit modernsten Methoden und Analyseinstrumenten durchgeführt. Auf molekularer Ebene untersuchen wir Target-Ligand-Interaktionen mit verschiedenen biophysikalischen Techniken wie SPR, MST, FP, ITC, STD-NMR, Röntgenkristallographie sowie computergestützten Methoden, z. B. Molekulardocking und Molekulardynamik (MD) Simulation. Wir charakterisieren molekulare Wechselwirkungen hinsichtlich Art, Stärke, Geometrie und beteiligten Atomen oder funktionellen Gruppen, um den MoA zu verstehen und die Affinität sowie Selektivität der Verbindung zu optimieren.
Forschungsprojekte
BAM
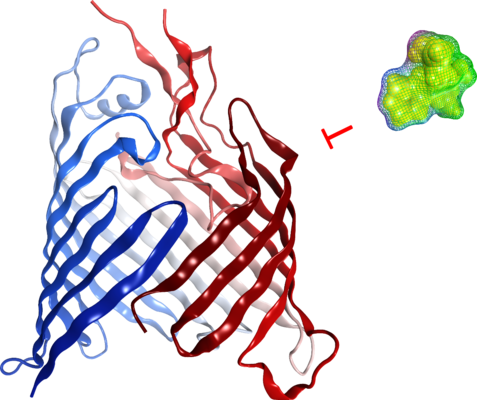
Die β-Barrel-Assemblierungsmaschine (BAM) ist ein Membranprotein mit mehreren Untereinheiten, das für die Biogenese der äußeren Membran (OM) bei Gram-negativen Bakterien von entscheidender Bedeutung ist. Interferenz mit BAM ist eine attraktive Strategie zur Entwicklung eigenständiger Antibiotika gegen die herausfordernden Gram-negativen Bakterien. Wir haben computergestütztes Wirkstoffdesign (CADD)-Ansätze angewendet, um neuartige synthetische kleine Moleküle mit günstigem Aktivitätsprofil zu identifizieren. Struktur-Aktivitäts-Beziehungsstudien (SAR) werden für die Hitoptimierung entwickelt.
IRG1
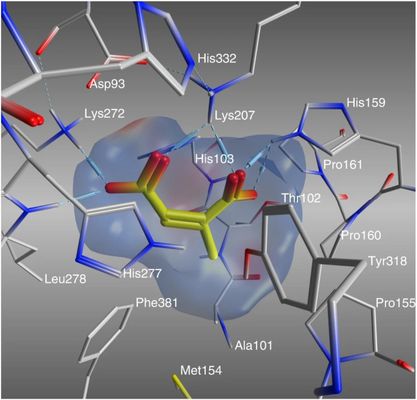
Das humane immun-responsive Gen 1 (IRG1), auch bekannt als cis- Aconitatdecarboxylase (ACOD1), ist ein mitochondriales Enzym, das bei bakteriellen und viralen Infektionen, Sepsis, Entzündungen sowie Tumoren hochreguliert ist. Es katalysiert die Umwandlung von cis-Aconitsäure in Itaconsäure, einem endogenen immunmodulatorischen Metaboliten, der mit Immunerschöpfung in Verbindung gebracht wurde. Die Hemmung von IRG1 schützt nachweislich vor mikrobiellen Infektionen und verhindert Tumorwachstum in vivo, was IRG1 als vielversprechendes therapeutisches Target für die Entwicklung von Wirt-gerichteten antiinfektiösen und immunprotektiven Wirkstoffe hervorhebt. Wir haben sowohl struktur- als auch ligandenbasierte Designkampagnen zur multidimensionalen Optimierung neuartiger IRG1-Modulatoren mit deutlich verbesserten Aktivitäten im Vergleich zum ersten natürlichen Ligand Citraconsäure (CA) durchgeführt, den wir kürzlich entdeckt haben. Molekulare Wechselwirkungen werden anhand von ITC- und Röntgenkristallstrukturen bewertet. Unsere Lead-Kandidaten werden in einer Proof-of-Concept-Studie (PoC) auf ihre antiinfektiösen und zytoprotektiven Wirkungen in Tiermodellen untersucht (in Zusammenarbeit mit HZI und UdS).
Publikationen
Einen Überblick über Walid A. M. Elgahers Veröffentlichungen finden Sie auf seiner persönlichen Seite.